|
|
Cepas de Rhizobium spp. con potencial biofertilizante: selección multivariada y su tolerancia a condiciones críticas de suelos tropicales
Kenneth Segura-Hidalgo1![]() , Lidieth Uribe-Lorío2
, Lidieth Uribe-Lorío2![]()
1. Universidad de Costa Rica, Centro de Investigaciones Agronómicas, Montes de Oca, San José, Costa Rica; kenneth.segurahidalgo@ucr.ac.cr
2. Universidad de Costa Rica, Centro de Investigaciones Agronómicas, Escuela de Agronomía, Montes de Oca, San José, Costa Rica; lidieth.uribe@ucr.ac.cr
Recibido 29-I-2026 ● Corregido 13-IV-2026 ● Aceptado 06-V-2026
DOI: https://doi.org/10.22458/urj.v18i1.6363
ABSTRACT. “Rhizobium spp. strains with biofertilizer potential: Multivariate selection and their tolerance to critical conditions of tropical soils” Introduction: Leguminous plants establish symbiotic relationships with bacteria of the genus Rhizobium, which represent an important source of organic nitrogen in sustainable production. However, successful bacterial colonization remains a challenge due to the variability of soil conditions and current agronomic practices. Objective: To select Rhizobium spp. strains based on their tolerance to salinity and aluminum toxicity, and to evaluate their effect on the foliar mineral content of common bean (Phaseolus vulgaris). Methods: We did triplicate assays on Rhizobium spp. strains, from a Costa Rican laboratory, selected for siderophore production, phosphorus solubilization, and tolerance to salinity and aluminum toxicity. In greenhouse, we filled 4-L pots with soil that had been autoclaved twice. We inoculated seeds of the Guaymí and Cabécar varieties at sowing with the selected strains at a concentration of 10⁸ CFU. We established five treatments: T1 (CIAT899), T2 (CR4019B), T3 (CIAT899 + CR4019B), T4 (urea), and T5 (control), with four replicates in a randomized design. We terminated the experiment at flowering and analyzed foliar tissue chemistry. Results: Salinity was a major limiting factor for most strains, and aluminum exposure restricted growth. The strains CIAT899 and CR4019B had high phosphorus solubilization and lower siderophore production. Inoculation increased foliar nitrogen content in both varieties and resulted in significant differences in calcium, zinc, and boron in the Guaymí variety, with no differences in foliar nitrogen compared to the urea treatment. Conclusion: Responses depend on cultivar, emphasizing the need to select compatible strains and genotypes. Overall, Rhizobium spp. offers a sustainable alternative because inoculation with selected strains (particularly CIAT899 and CR4019B), enhances phosphorus solubilization and siderophore production, improving the availability and uptake of essential nutrients in P. vulgaris, including foliar nitrogen levels comparable to those achieved with synthetic fertilizers (urea), as well as good levels of calcium, zinc, and boron.
Keywords: nitrogen, phosphorus, siderophores, abiotic stress, tropical soils.
RESUMEN. Introducción: las leguminosas establecen relaciones simbióticas con bacterias del género Rhizobium spp., una importante fuente de nitrógeno orgánico en la producción sostenible. Sin embargo, la colonización bacteriana exitosa sigue siendo un desafío debido a la variabilidad del suelo y las prácticas agronómicas actuales. Objetivo: seleccionar cepas de Rhizobium spp. según su tolerancia a salinidad y toxicidad por aluminio, y evaluar su efecto sobre el contenido mineral foliar del frijol común (Phaseolus vulgaris). Métodos: realizamos ensayos por triplicado con cepas de Rhizobium spp. de un laboratorio costarricense, seleccionadas por producción de sideróforos, solubilización de fósforo y tolerancia a salinidad y toxicidad por aluminio. En invernadero, llenamos macetas de 4L con suelo autoclavado dos veces. Inoculamos semillas de las variedades guaymí y cabécar al momento de la siembra con las cepas seleccionadas a una concentración de 10⁸ UFC. Establecimos cinco tratamientos: T1 (CIAT899), T2 (CR4019B), T3 (CIAT899 + CR4019B), T4 (urea) y T5 (control) con cuatro repeticiones en un diseño aleatorizado. Finalizamos el experimento en floración y analizamos la química del tejido foliar. Resultados: la salinidad fue un factor limitante importante para la mayoría de las cepas y la exposición al aluminio restringió el crecimiento. Las cepas CIAT899 y CR4019B presentaron alta solubilización de fósforo y menor producción de sideróforos. La inoculación aumentó el contenido foliar de nitrógeno en ambas variedades y produjo diferencias significativas en calcio, zinc y boro en la variedad guaymí sin diferencias en nitrógeno foliar respecto al tratamiento con urea. Conclusión: las respuestas dependen de su cultivo, lo que resalta la necesidad de seleccionar cepas y genotipos compatibles. En general, Rhizobium spp. ofrece una alternativa sostenible, dado que la inoculación con cepas seleccionadas, especialmente CIAT899 y CR4019B, mejoran la solubilización de fósforo y la producción de sideróforos que favorecen la disponibilidad y absorción de nutrientes esenciales en P. vulgaris, incluido el nitrógeno foliar comparable al logrado con fertilizantes sintéticos (urea), así como buenos niveles de calcio, zinc y boro.
Palabras clave: nitrógeno, fósforo, sideróforos, estrés abiótico, suelos tropicales.
La simbiosis que las plantas de frijol establecen con las bacterias del género Rhizobium ofrece una fuente de nitrógeno importante para el desarrollo de la planta y el contenido de proteína del grano; sin embargo, esta relación se ve afectada por el aumento de la salinidad del suelo como resultado del uso continuo de fertilizantes sintéticos (Pahalvi et al., 2021).
Ensayos realizados en Costa Rica muestran que la salinidad, aún en bajas concentraciones, ocasiona la reducción de hasta un 90% en la cantidad de nódulos efectivos en cepas con baja tolerancia (Ballhorn et al., 2018). La salinización de suelos es un peligro inminente dada la alta dependencia de sales minerales para la fertilización de los cultivos (Pla Sentís, 2020; Sanga et al., 2024), aunado a los programas de riego cada vez más necesarios debido al cambio en los patrones de lluvia (Mamalakis et al., 2021; Utsumi & Kim, 2022).
Desde la década de los 90, en Guanacaste, una provincia agrícola con un alto uso de aguas de riego debido a sus condiciones climáticas, se han reportado indicios de un alza en la salinidad de los suelos (Montes de Oca et al., 1996). Algunas cepas de Rhizobium han mostrado tolerancia a la salinidad (Wekesa et al., 2022) y al aluminio (Fahde et al., 2023) lo que las hace una excelente opción para el uso en los sistemas agrícolas.
Tanto las bacterias como otros microorganismos pueden promover el crecimiento vegetal al solubilizar elementos claves como el hierro y el fósforo que, a pesar de su abundancia en la corteza terrestre, se encuentran en estado insoluble con una baja solubilización natural (Bindraban et al., 2020; Waring et al., 2021). Para solventar esto, ciertas cepas de Rhizobium spp. tienen la capacidad de producir sustancias con alta afinidad por el hierro llamadas sideróforos que permiten la solubilización del hierro (Galvis Serrano et al., 2024) y la producción de ácidos orgánicos que permiten la liberación de fósforo (Portillaϯ et al., 2025).
Estas características permiten aprovechar los recursos del suelo sin la adición de compuestos sintéticos, enfocándose en una agricultura más sostenible y con responsabilidad ecológica (García-Berumen et al., 2024; Timofeeva et al., 2023). Nuestro objetivo fue evaluar la resistencia de las cepas de Rhizobium spp. de la colección del Laboratorio de Microbiología Agrícola a condiciones de salinidad y presencia de aluminio, típicas de suelos tropicales, así como su capacidad para solubilizar Fe y P que se encuentra ligado a otros minerales de suelo.
MATERIALES Y MÉTODOS
El ensayo lo llevamos a cabo en el invernadero del Laboratorio de Microbiología Agrícola (LMA) del Centro de Investigaciones Agronómicas de la Universidad de Costa Rica, entre agosto y septiembre del año 2024. Tomamos 20 cepas de Rhizobium de la colección del Laboratorio de Microbiología Agrícola (LMA) y realizamos una selección que consistió en evaluar su tolerancia a la salinidad y a diferentes concentraciones de aluminio, así como la capacidad para solubilizar fósforo y la producción de sideróforos para la liberación de hierro. La tolerancia a la salinidad se determinó mediante la capacidad de las cepas para crecer a diferentes concentraciones de NaCl mediante inoculación de las cepas de Rhizobium spp., en el medio Agar Levadura Manitol (ALM): (Manitol: 10g/L; extracto de levadura: 2g/L; K2HPO4: 0,5g/L; MgSO4 7H2O: 0,1g/L; agar bacteriológico: 5g/L; 10mL/L de rojo Congo al 0,25%; agua desionizada: 1L) suplementado con NaCl a 25, 50, 75 y 100mM. Cada plato se dividió en cuatro secciones y cada bacteria se inoculó con un asa bacteriológica estéril por picadura con tres repeticiones en platos diferentes. Los platos se incubaron a temperatura ambiente por tres días. Se evaluó el crecimiento mediante una escala visual de 0 (sin respuesta) a 4 (crecimiento en toda la línea de rayado).
Tolerancia a diferentes concentraciones de aluminio: el ensayo lo realizamos de acuerdo con la metodología descrita por Castillo R et al., (2008). Se preparó caldo levadura manitol y se le adicionó una solución de AlCl3 6∙H2O 1000μM en dosis equivalentes a 22,3μM Al, 44,7μM Al y 67,0μM Al. Todos los medios de cultivo suplementados con Al se llevaron a un pH de 5,5, utilizando HCl 1M. Los incubamos en baño de María con agitación constante por 48 horas a 28°C y 60rpm. Medimos la absorbancia a 620nm en un espectrofotómetro BK-UV/Vis.
Solubilización de P: utilizamos cuatro medios de cultivo para evaluar la capacidad de las cepas para utilizar fuentes diferentes de P. El Medio Agar Pikovskaya contiene: extracto de levadura: 0,5g/L; D-glucosa: 10g/L; Ca₃(PO₄)₂: 5g/L; (NH₄)₂SO₄: 0,5g/L; KCl: 0,2g/L; MgSO₄: 0,1g/L; MnSO₄: 0,0001g/L; FeSO₄: 0,0001g/L; agar bacteriológico: 15g/L; agua desionizada: 1L; pH: 6,8. Por otro lado, el Medio de Osorio & Habte (2001) que contiene: NaCl: 1g/L; CaCl₂·2H₂O: 0,2g/L; MgSO₄·7H₂O: 0,4g/L; NH₄NO₃: 0,2g/L; D-glucosa: 10g/L; roca fosfórica: 3,5g/L; agar bacteriológico: 15g/L; agua desionizada: 1L; verde de bromocresol: 30mg/L; pH: 6,8. Para el medio de Gadagi & Sa (2002): D-glucosa 10g/L; NaCl: 0,1g/L; MgSO₄·7H₂O: 0,5g/L; extracto de levadura: 0,2g/L; NH₄Cl: 0,5g/L; MnSO₄·H₂O: 0,1g/L; K₂HPO₄: 0,5g/L; agar bacteriológico: 15g/L; agua desionizada: 1L; verde de bromocresol: 30mg/L; fosfato de hierro (FePO₄): 2g/L; fosfato de aluminio (AlPO₄): 5g/L. El medio Pikovskaya utiliza como fuente de fósforo insoluble el Ca3(PO4)2 (P. Singh et al., 2014) y la capacidad de solubilizar fosfatos se visualiza por la formación de un halo transparente alrededor del crecimiento bacteriano (Sigma-Aldrich, 2013). Por su parte el medio desarrollado por Osorio & Habte (2001) utiliza roca fosfórica como fuente de fósforo y verde de bromocresol como indicador de pH (Silva et al., 2001), la solubilización de P se detecta mediante la formación de un halo de color amarillo. Por último, utilizamos un medio base modificado para determinar la solubilización de fosfatos de hierro y aluminio mediante el cambio de color de azul a anaranjado (Gadagi & Sa, 2002; Reyes et al., 1999). El ensayo lo realizamos por triplicado y en cada plato se inoculó con una gota de 10μL de una suspensión de cada cepa. Preparamos la suspensión a partir del crecimiento de tres días en el medio ALM con rojo Congo a temperatura ambiente. Se evaluó de manera visual de 0 (sin respuesta) a 4 (máxima respuesta).
Producción de sideróforos: utilizamos la metodología descrita por Milagres et al., (1999). Inoculamos las cepas en platos de medio de cultivo que contenían en una mitad el medio ALM y en la otra el medio cromo azurol S (CAS). La presencia de sideróforos fue determinada mediante el cambio en el color del medio CAS de un azul intenso a tonos pardo-rojizos o amarillo, partiendo del límite entre los dos medios. El cambio de color se debe a la remoción del hierro del complejo Fe-CAS por los sideróforos producidos por las bacterias, lo que ocasiona un viraje de azul a tonos anaranjados (Alexander & Zuberer, 1991). Se evaluó de manera visual de 0 (sin respuesta) a 4 (máxima respuesta).
Selección de cepas: para evaluar integralmente la capacidad de promoción de crecimiento y la tolerancia al estrés abiótico de las cepas, se desarrolló el índice de selección que consta de tres fases. 1 cuantificación y normalización: los datos brutos fueron normalizados en un rango de cero a uno mediante la técnica de escalamiento lineal, donde x es el valor observado, Xmax y Xmin representan los valores máximos y mínimos.
![]()
2. Ponderación de atributos: se le otorgó un peso específico a cada variable según la relevancia agronómica en suelos ácidos, de esta manera, el índice de selección contabiliza una relevancia del 35% para la producción de sideróforos, 35% para la solubilización de fósforo, 15% para la tolerancia al aluminio y 15% para la tolerancia a la salinidad. 3. Para representar la variabilidad biológica en el ranking final se realizó una propagación de la incertidumbre. El error estándar del índice de selección se calculó a partir de los errores estándares de los componentes individuales y sus respectivos pesos.
Análisis foliar. Para el ensayo de invernadero utilizamos suelo autoclavado a 120°C por una hora en dos ocasiones, con el fin de asegurarse de que no hubiera microorganismos fijadores de nitrógeno que pudieran interferir con el estudio. El suelo autoclavado lo dejamos reposar durante ocho días para que se estabilizara y se llenaron macetas de 4L.
Inoculamos con las dos cepas de Rhizobium spp. con la mejor puntuación al momento de la siembra con una suspensión de 10mL y una concentración de 108UFC/mL de Rhizobium, en cinco tratamientos T1(CIAT899), T2(CR4019B), T3(CIAT899 + CR4019B), T4(urea) y T5(testigo) con cuatro repeticiones cada uno distribuidos de forma aleatoria al azar. Utilizamos semillas de frijol de las variedades cabécar y guaymí a razón de cinco semillas por maceta con un raleo a los 15 días para dejar dos plantas por maceta. El ensayo lo terminamos a inicios de floración (R6) y enviamos una muestra de tejido foliar al Laboratorio de Suelos y Foliares de la UCR para un análisis químico completo.
Análisis estadístico: las variables medidas mediante escala visual las analizamos con una estadística no paramétrica debido a la naturaleza de los datos. Utilizamos la prueba de Kruskal-Wallis (p < 0,05) y cuando detectamos diferencias significativas aplicamos la prueba de post hoc de Dunn con el método de ajuste de Benjamini-Hochberg para comparaciones múltiples. Y para analizar el efecto de las distintas variables aplicamos la prueba de Friedman (p < 0,05).
Para evaluar la tolerancia de las cepas a las concentraciones crecientes de aluminio, determinamos el Área Bajo la Curva (ABC) calculada a partir de la respuesta biológica en cuatro niveles de tratamientos (T0 a T3) en dosis crecientes. El cálculo del ABC lo realizamos mediante el método de integración trapezoidal que permite consolidar la respuesta a la gradiente de estrés en un único parámetro cuantitativo de resiliencia.
Las diferencias significativas entre las cepas se determinaron mediante un análisis de varianza. En los casos en los que determinamos diferencias significativas (p< 0,05), se procedió a realizar una prueba de comparaciones múltiples de Tuckey para agrupar las cepas según su nivel de tolerancia. Todas las pruebas de selección contaron con tres repeticiones.
Los datos del ensayo de invernadero se analizaron mediante un análisis de varianza y una comparación de media mediante LSD Fisher (p<0,05). Los platos se dispusieron para las pruebas de laboratorio bajo un diseño completamente al azar, de igual forma, en el ensayo de invernadero las macetas también se ubicaron al azar para garantizar la independencia de las observaciones. Todos los datos los analizamos en el programa R Studio 2026.01.0 Build 392.
RESULTADOS
La prueba de tolerancia a la salinidad mostró afectación en el crecimiento de la bacteria desde la concentración más baja de NaCl evaluada. El crecimiento disminuyó notablemente a partir de los 50mM, de manera que sólo dos cepas mantuvieron un crecimiento óptimo a los 100mM. Las cepas CIAT899, CR4014B y CR4019B crecieron a concentraciones salinas desde los 25mM hasta los 50mM de NaCl. A la máxima salinidad evaluada, las cepas CR4001B, CR4007B, CR4010B, CR4011B, CR4012B y CR4018B mostraron una tolerancia media, mientras que las cepas CR4014B y CR4019B se identificaron como las cepas con mejor tolerancia a 10 mM de NaCl (Fig. 1).
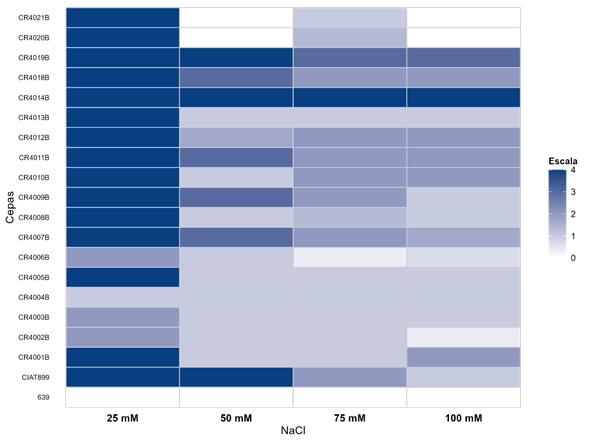
Fig. 1. Tolerancia a la salinidad de 20 cepas de Rhizobium spp. en medio sólido Agar Levadura Manitol (ALM) adicionado con 25, 30, 35 y 40mM NaCl incubadas a temperatura ambiente durante tres días.
En términos generales, la salinidad en el medio afectó la media de todas las cepas evaluadas con diferencias significativas (p < 0,001) entre los 75 y 10 mM de NaCl (Fig. 2).
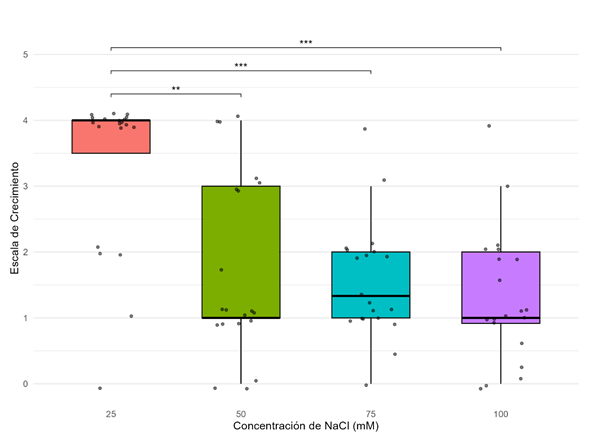
Fig. 2. Tolerancia a la salinidad de cepas de Rhizobium spp. Los valores representan el promedio de respuesta de n= 20 cepas. Las barras superiores indican las comparaciones pareadas significativas según la prueba de rangos de Wilcoxon (ajuste de holm) tras detectar diferencias globales con la prueba de Friedman (p < 0,05). Niveles de significancia: *p: < 0,05; **p: < 0,01; ***p < 0,001).
Otro factor típico en suelos tropicales es la toxicidad por aluminio (Fig. 3), en este escenario, la sensibilidad de las bacterias difirió entre cada una de las cepas, algunas como la CR4021B mostraron una disminución drástica en su crecimiento con el aumento en la concentración de Al3+, otras como las CR4019B, CR4004B, CR4001B y la CR4006B repuntan como las cepas con mejor tolerancia.
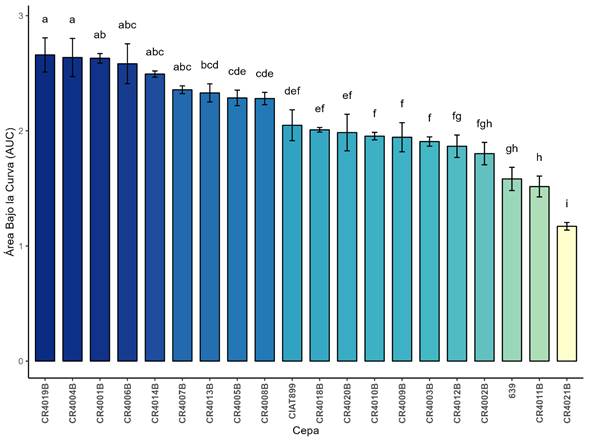
Fig. 3. Respuesta de 20 cepas de Rhizobium spp. a dosis crecientes de aluminio. Los valores representan el promedio del Área Bajo la Curva, las barras de error indican la desviación estándar (n=3). Las letras diferentes indican diferencias estadísticamente significativas (p<0,05) de acuerdo con el análisis de varianza y la prueba de comparaciones múltiples de Tuckey.
En cuanto a la solubilización de P, encontramos que una gran mayoría de las cepas de Rhizobium spp. evaluadas fueron capaces de solubilizar el fósforo en el medio de Osorio & Habte (2001), seguido por los medios cuya fuente de fósforo eran fosfatos de hierro, aluminio y, por último, el Medio Pikoskaya (Fig. 4), en el que sólo seis cepas fueron capaces de solubilizar el P. Las cepas que no solubilizaron P en los medios con fosfatos de Fe y Al, si lo hicieron en el medio de Osorio.
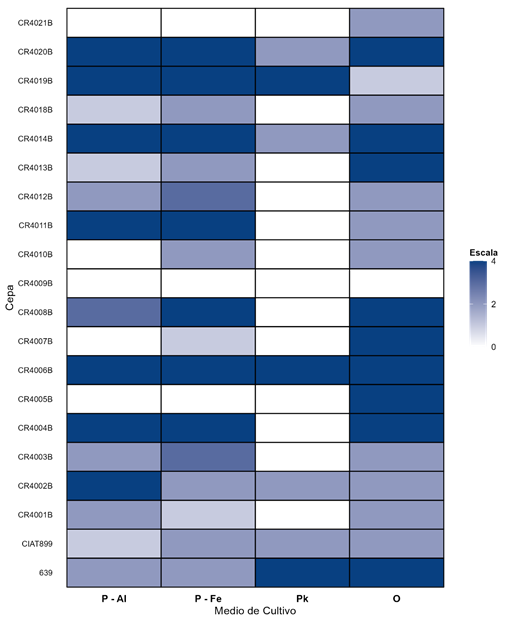
Fig. 4. Capacidad de solubilización de fósforo de 20 cepas de Rhizobium spp., en medio sólido incubadas a temperatura ambiente (O= Osorio y Habte 2002; Pk = Pikovskaya; P-Fe = fosfato de hierro; P-Al = fosfatos de aluminio).
La prueba de Friedman muestra que el Medio Pikovskaya se comporta de manera diferente a todos los demás medios evaluados (p<0,05), debido a que presentó la menor cantidad de resultados positivos (Fig. 5).
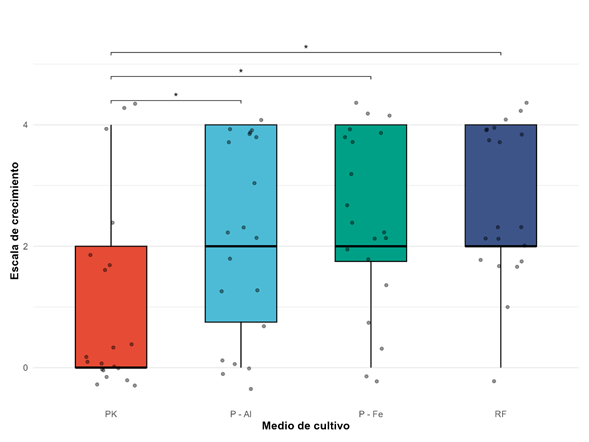
Fig. 5. Capacidad de solubilización de fósforo por cepas de Rhizobium spp. en cuatro medios distintos. Los valores representan el promedio de respuesta de n= 20 cepas. Las barras superiores indican las comparaciones pareadas significativas según la prueba de rangos de Wilcoxon (ajuste de Holm) tras detectar diferencias globales con la prueba de Friedman (p < 0,05).
Finalmente, encontramos que las cepas CIAT899, CR4001B, CR4003B, CR4010B, CR4011B, CR4012B, CR4013B y CR4019BB (Fig. 6) produjeron sideróforos en el medio CAS. Tal y como lo menciona Milagres et al. (1999), la sustracción del hierro acomplejado en el medio CAS genera el cambio de color de azul a tonos rojizos, en este caso por parte de la Rhizobium spp. al avanzar desde su punto de inoculación (Fig. 6D) hacia el extremo opuesto del plato. El mayor viraje del medio se obtuvo en las cepas CR4012B, CR4001B, CR4003B y CR4010B en orden decreciente de la mejor respuesta hacia la menor.
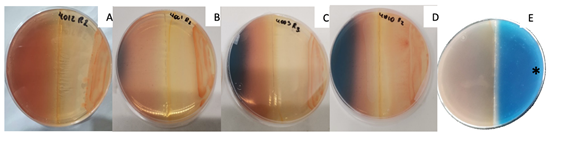
Fig. 6. Producción de sideróforos en cepas de Rhizobium spp., (A= CR4012B; B= CR4001B; C = CR4003B; D = CR4010B; E = plato de referencia sin inocular).
De acuerdo con los criterios de selección establecidos, la cepa CR4019B repunta como la mejor, seguida de cerca por la CIAT899 (Fig. 7). Sin embargo, se nota claramente un grupo que incluye, además, a las cepas CR4013B, CR4001B, CR4012B, CR4014B, CR4003B y CR4011B, las cuales se distinguen por las cualidades evaluadas entre las que resaltan la capacidad de producción de sideróforos y la solubilización de fósforo. Resulta notable que el 50% de las cepas evaluadas presenta un índice de selección inferior a 0,5, lo que sugiere que los rasgos de interés no se encuentran distribuidos uniformemente y representan cualidades especializadas presentes en una fracción de la diversidad bacteriana evaluada y debido a que son de gran interés para la agricultura se convierten en cualidades valiosas por explorar.
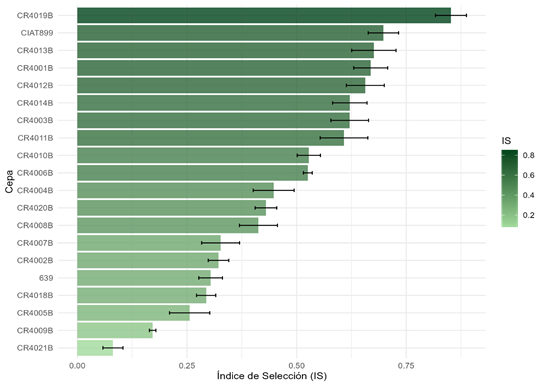
Fig. 7. Índice de selección para las cepas de Rhizobium spp. El índice integra la capacidad de solubilización de fosforo (35%), producción de sideróforos (35%), tolerancia a la salinidad (15%) y el aluminio (15%). Las barras de error indican la desviación estándar. Los valores cercanos a uno indican un mayor potencial multivariado para la promoción de crecimiento vegetal.
El análisis foliar (TABLA 1) muestra que el contenido de nitrógeno presentó diferencias significativas en la variedad Cabécar del T1 (CIAT899) con el T5 (testigo), mientras que en la variedad guaymí no hay diferencias. El fósforo, de igual manera que el nitrógeno, presentó diferencias significativas en la variedad cabécar del T1 (CIAT899) con el T5 (testigo) y en la variedad guaymí el T2 (CR4019B) presenta diferencias con el T5 (testigo). El calcio sólo presentó diferencias en la variedad guaymí del T1 (CIAT899) con los tratamientos no inoculados T4 (urea) y T5 (testigo). Por su parte el Zn y el B muestran diferencias en la variedad guaymí del T1 (CIAT899) y el T2 (CR4019B) con el T5 (testigo).
TABLA 1
Efecto de Rhizobium spp. sobre el contenido de minerales en el tejido foliar de frijol (Phaseolus vulgaris L.)
|
Variedad |
Tratamiento |
N (%) |
P (%) |
K (%) |
Ca (mg/Kg) |
Zn (mg/Kg) |
B (mg/Kg) |
|
C |
T1 |
6,0 A |
0,5 A |
5,3 A |
1,9 AB |
52,7 BC |
34,3 ABC |
|
C |
T2 |
5,6 ABC |
0,5 AB |
4,7 AB |
1,6 B |
47,3 C |
36,0 AB |
|
C |
T3 |
5,5 ABCD |
0,4 ABCD |
5,0 AB |
1,8 AB |
57,0 BC |
29,3 C |
|
C |
T4 |
5,3 BCD |
0,5 ABC |
5,2 AB |
1,6 B |
53,3 BC |
33,3 BC |
|
C |
T5 |
5,0 D |
0,4 CD |
4,8 AB |
1,6 B |
46,3 C |
34,3 ABC |
|
G |
T1 |
5,6 ABC |
0,4 ABCD |
5,1 AB |
2,1 A |
71,0 A |
35,7 AB |
|
G |
T2 |
5,8 AB |
0,5 A |
5,0 AB |
1,7 B |
65,7 AB |
39,7 A |
|
G |
T3 |
5,0 CD |
0,4 D |
4,8 AB |
1,8 AB |
60,0 ABC |
31,0 BC |
|
G |
T4 |
5,4 ABCD |
0,5 A |
4,6 AB |
1,7 B |
60,0 ABC |
35,0 ABC |
|
G |
T5 |
5,4 BCD |
0,4 BCD |
4,5 B |
1,5 B |
51,0 C |
29,3 C |
C= cabécar; G= guaymí; T1 = CIAT899; T2= CR4019BB; T3= CIAT899 + CR4019BB; T4= urea, T5= testigo. Medias con letra común no son significativamente diferentes según la prueba de diferencias mínima de LSD Fisher (p < 0,05).
DISCUSIÓN
La tolerancia a la salinidad de la cepa CIAT899 (Fig. 1) es consistente con lo reportado por Fernandez-Aunián et al., (2010), quienes determinaron su óptimo desarrollo a 50mM de NaCl y una tolerancia máxima hasta 200mM. La importancia de obtener cepas con tolerancia a la salinidad radica en su capacidad de transmitir parte de esta tolerancia a la planta huésped y, de esta manera, mejorar su crecimiento antes tales condiciones (Wekesa et al., 2022).
Otro punto limitante en los suelos tropicales es la disponibilidad de fósforo, debido a que gran parte de él se encuentra unido a óxidos metálicos de Fe y Al (Johan et al., 2021). Con respecto a este punto y conociendo la amplia demanda de fósforo requerida para realizar la fijación biológica de nitrógeno, las bacterias fijadoras de nitrógeno que posean los mecanismos para solubilizar este elemento tendrán una ventaja competitiva (Bardin et al., 1996; Rees et al., 2005). Los resultados obtenidos muestran que la mayoría de las cepas evaluadas puede solubilizar fosfatos de Fe y Al, además de fosfatos de Ca. Lo que representa una característica importante para su uso en los biofertilizantes (Shome et al., 2022). Es importante aclarar que el uso de diferentes medios para la selección de bacterias con potencial para solubilizar fósforo ofrece un criterio más amplio para la toma de decisiones y un mejor desempeño en el campo (Bashan et al., 2013a, 2013b; Jones & Oburger, 2011).
En cuanto a la producción de sideróforos, sólo un 40% de las cepas evaluadas mostraron una respuesta positiva, por lo que se considera una característica poco común entre las cepas de Rhizobium spp. evaluadas (Ben Romdhane et al., 2022; Sulistiyani et al., 2024); sin embargo, su importancia puede ir más allá de la biofortificación del Fe en la planta y generar competencia por este mineral con otros microrganismos, entre los cuales se pueden citar hongos fitopatógenos habitantes del suelo como Fusarium spp. (Das et al., 2017; Verma et al., 2019), por lo que esta característica se vuelve de gran interés.
El aluminio en el suelo representa una limitante para el establecimiento de la simbiosis entre Rhizobium spp. y las leguminosas (Artigas Ramírez et al., 2018; Mmayi & Musyimi, 2025). Los ensayos realizados con la cepa CIAT899 muestran que puede presentar una tolerancia hasta los 100μM de Al (Ferreira et al., 2012), lo que concuerda con nuestros datos, al lado de cepas como la CR4019B con una muy buena tolerancia a la exposición al aluminio. Esta tolerancia se les atribuye a mecanismos internos de la bacteria que permiten la reparación y estabilización de las membranas celulares en condiciones de estrés por altas concentraciones de Al (Wekesa et al., 2022).
Nuestros datos indican que la inoculación con Rhizobium spp. genera diferencias significativas (p<0,05) en la concentración de nitrógeno foliar en las plantas de frijol, comparado con el tratamiento sin inocular, esto es un indicador de que la fijación biológica es capaz de sostener los requerimientos de producción y de compararse con los resultados obtenidos con la aplicación de nitrógeno sintético aplicado al campo (Bērtiņš et al., 2021), cuya producción requiere grandes cantidades de energía y deja una gran huella de carbono (Masjedi et al., 2024).
La diferencia en la respuesta en el contenido foliar de minerales de las dos variedades evaluadas ante la inoculación puede deberse a características propias de la relación simbiótica, dado que durante su establecimiento se produce una serie de intercambios de sustancias, cuyo propósito es la atracción de la bacteria. Durante los procesos de mejoramiento genético muchas plantas sufrieron un desgaste en su interacción con los microorganismos del suelo en beneficio de una mayor producción (Garcha & Garcha, 2023) y esto podría explicar por qué la variedad cabécar no presenta diferencias en el contenido de boro y calcio, caso contrario a la variedad guaymí.
De acuerdo con el IS el grupo de cepas que abarca desde la CR4019B y CIAT899 hasta la CR4013B, CR4001B, CR4012B, CR4014B, CR4003B y CR4011B representan las mejores candidatas para ser evaluadas en campo por su buen desempeño de acuerdo con las características evaluadas. Estas características pueden conferir a la planta una mejor interacción con el suelo y los minerales que se encuentran en estado insoluble en las partículas del suelo, lo que confiere un potencial para mejorar la nutrición de la planta mediante la inoculación con microorganismos, una técnica que busca una agricultura sostenible y responsable (Ammar et al., 2023; Fiodor et al., 2021; M. Singh et al., 2025).
Los resultados obtenidos podrían servir como una guía para la elaboración de un biofertilizante que ayude a reducir la cantidad de fertilizante fosfatado y de nitrógeno sintético con el manteniendo o incluso, un incremento en los rendimientos debido a la capacidad de solubilizar el fósforo acomplejado en el suelo (Samago & Dakora, 2024). Para futuras investigaciones sería importante explorar el efecto de Rhizobium spp. sobre el contenido foliar de minerales en plantas silvestres que cuentan con mayor rusticidad.
AGRADECIMIENTOS
Agradecemos al Laboratorio de Microbiología Agrícola del Centro de Investigaciones Agronómicas (CIA) por permitir y financiar esta investigación.
ÉTICA, CONFLICTO DE INTERESES Y DECLARACIÓN DE FINANCIAMIENTO
Los autores declaramos haber cumplido cabalmente con todos los requisitos éticos y legales pertinentes, tanto durante el estudio como en la producción del manuscrito; que no existen conflictos de intereses de ningún tipo; que todas las fuentes financieras estén completa y claramente indicadas en la sección de agradecimientos y que están totalmente de acuerdo con la versión final editada del artículo. Un documento firmado ha sido archivado en los archivos de la revista.
La declaración de contribución de cada autor es la siguiente: K.S.H: Recolección, análisis de datos y preparación y aprobación final del manuscrito. L.U.L: Asesoría en todo el proceso investigativo, preparación y aprobación final del manuscrito.
REFERENCIAS
Alexander, D. B., & Zuberer, D. A. (1991). Use of chrome azurol S reagents to evaluate siderophore production by rhizosphere bacteria. Biology and Fertility of Soils, 12(1), 39–45. https://doi.org/10.1007/BF00369386
Ammar, E. E., Rady, H. A., Khattab, A. M., Amer, M. H., Mohamed, S. A., Elodamy, N. I., AL-Farga, A., & Aioub, A. A. A. (2023). A comprehensive overview of eco-friendly bio-fertilizers extracted from living organisms. Environmental Science and Pollution Research International, 30(53), 113119. https://doi.org/10.1007/s11356-023-30260-x
Artigas Ramírez, M. D., Silva, J. D., Ohkama-Ohtsu, N., & Yokoyama, T. (2018). In vitro rhizobia response and symbiosis process under aluminum stress. Canadian Journal of Microbiology, 64(8), 511–526. https://doi.org/10.1139/cjm-2018-0019
Ballhorn, D. J., Wolfe, E. R., Tyler, J., Ronan, W., & Sands-Gouner, S. (2018). Quantitative Effects of Soil Salinity on the Symbiosis of Wild Lima Bean (Phaseolus lunatus L.) and Bradyrhizobium in Costa Rica. Journal of Applied Botany and Food Quality, (91), 304–309. https://doi.org/10.5073/JABFQ.2018.091.039
Bardin, S., Dan, S., Osteras, M., & Finan, T. M. (1996). A phosphate transport system is required for symbiotic nitrogen fixation by Rhizobium meliloti. Journal of Bacteriology, 178(15), 4540–4547. https://doi.org/10.1128/JB.178.15.4540-4547.1996
Bashan, Y., Kamnev, A. A., & de-Bashan, L. E. (2013a). A proposal for isolating and testing phosphate-solubilizing bacteria that enhance plant growth. Biology and Fertility of Soils, 49(1), 1–2. https://doi.org/10.1007/s00374-012-0756-4
Bashan, Y., Kamnev, A. A., & de-Bashan, L. E. (2013b). Tricalcium phosphate is inappropriate as a universal selection factor for isolating and testing phosphate-solubilizing bacteria that enhance plant growth: a proposal for an alternative procedure. Biology and Fertility of Soils, 49(4), 465–479. https://doi.org/10.1007/s00374-012-0737-7
Ben Romdhane, S., De Lajudie, P., Fuhrmann, J. J., & Mrabet, M. (2022). Potential role of rhizobia to enhance chickpea-growth and yield in low fertility-soils of Tunisia. Antonie van Leeuwenhoek, International Journal of General and Molecular Microbiology, 115, 921–932. https://doi.org/10.1007/s10482-022-01745-5
Bērtiņš, M., Klūga, A., Dubova, L., Petrēvics, P., Alsiņa, I., & Vīksna, A. (2021). Study of Rhizobia Impact on Nutritional Element Concentration in Legumes. Proceedings of the Latvian Academy of Sciences. Section B. Natural, Exact, and Applied Sciences, 75(6), 457–462. https://doi.org/10.2478/prolas-2021-0068
Bindraban, P. S., Dimkpa, C. O., & Pandey, R. (2020). Exploring phosphorus fertilizers and fertilization strategies for improved human and environmental health. In Biology and Fertility of Soils (Vol. 56, pp. 299–317). Springer. https://doi.org/10.1007/s00374-019-01430-2
Castillo R, C. G., Rubio H, R., Urzúa S, H., & Borie B, F. (2008). Interacción Rhizobium leguminosarum bv trifolii y hongos micorrícicos en un andisol con diferentes niveles de saturación de aluminio. Idesia (Arica), 26(3), 7–19. https://doi.org/10.4067/S0718-34292008000300002
Das, K., Prasanna, R., & Saxena, A. K. (2017). Rhizobia: a potential biocontrol agent for soilborne fungal pathogens. In Folia Microbiologica (Vol. 62, pp. 425–435). Springer Netherlands. https://doi.org/10.1007/s12223-017-0513-z
Fahde, S., Boughribil, S., Sijilmassi, B., & Amri, A. (2023). Rhizobia: A Promising Source of Plant Growth-Promoting Molecules and Their Non-Legume Interactions: Examining Applications and Mechanisms. In Agriculture (Switzerland) (Vol. 13). Multidisciplinary Digital Publishing Institute (MDPI). https://doi.org/10.3390/agriculture13071279
Fernandez-Aunión, C., Hamouda, T. Ben, Iglesias-Guerra, F., Argandoña, M., Reina-Bueno, M., Nieto, J. J., Aouani, M. E., & Vargas, C. (2010). Biosynthesis of compatible solutes in rhizobial strains isolated from Phaseolus vulgaris nodules in Tunisian fields. BMC Microbiology, 10(1), 192. https://doi.org/10.1186/1471-2180-10-192
Ferreira, P. A. A., Bomfeti, C. A., Soares, B. L., & de Souza Moreira, F. M. (2012). Efficient nitrogen-fixing Rhizobium strains isolated from amazonian soils are highly tolerant to acidity and aluminium. World Journal of Microbiology and Biotechnology, 28(5), 1947–1959. https://doi.org/10.1007/S11274-011-0997-7/TABLES/3
Fiodor, A., Singh, S., & Pranaw, K. (2021). The Contrivance of Plant Growth Promoting Microbes to Mitigate Climate Change Impact in Agriculture. Microorganisms 2021, Vol. 9, Page 1841, 9(9), 1841. https://doi.org/10.3390/microorganisms9091841
Gadagi, R. S., & Sa, T. (2002). New isolation method for microorganisms solulbilizing iron and aluminum phosphates using dyes. Soil Science and Plant Nutrition, 48(4), 615–618. https://doi.org/10.1080/00380768.2002.10409246
Galvis Serrano, N. F., Moreno, L., Galvis Serrano, N. F., & Moreno, L. (2024). Sideróforos de rizobacterias y su aplicación en la biorremediación. Ciencia En Desarrollo, 15(2), 203–211. https://doi.org/10.19053/UPTC.01217488.V15.N2.2024.16996
Garcha, S., & Garcha, S. (2023). Microbes from Wild Plants. Metabolomics, Proteomes and Gene Editing Approaches in Biofertilizer Industry, 173–187. https://doi.org/10.1007/978-981-99-3561-1_10
García-Berumen, J. A., Flores de la Torre, J. A., de los Santos-Villalobos, S., Espinoza-Canales, A., Echavarría-Cháirez, F. G., & Gutiérrez-Bañuelos, H. (2024). Phosphorus dynamics and sustainable agriculture: The role of microbial solubilization and innovations in nutrient management. Current Research in Microbial Sciences, 8, 100326. https://doi.org/10.1016/J.CRMICR.2024.100326
Johan, P. D., Ahmed, O. H., Omar, L., & Hasbullah, N. A. (2021). Phosphorus Transformation in Soils Following Co-Application of Charcoal and Wood Ash. Agronomy 2021, Vol. 11, Page 2010, 11(10), 2010. https://doi.org/10.3390/AGRONOMY11102010
Jones, D. L., & Oburger, E. (2011). Solubilization of Phosphorus by Soil Microorganisms (pp. 169–198). https://doi.org/10.1007/978-3-642-15271-9_7
Mamalakis, A., Randerson, J. T., Yu, J. Y., Pritchard, M. S., Magnusdottir, G., Smyth, P., Levine, P. A., Yu, S., & Foufoula-Georgiou, E. (2021). Zonally contrasting shifts of the tropical rain belt in response to climate change. Nature Climate Change, 11, 143–151. https://doi.org/10.1038/s41558-020-00963-x
Masjedi, S. K., Kazemi, A., Moeinnadini, M., Khaki, E., & Olsen, S. I. (2024). Urea production: An absolute environmental sustainability assessment. Science of The Total Environment, 908, 168225. https://doi.org/10.1016/J.SCITOTENV.2023.168225
Milagres, A. M. F., Machuca, A., & Napoleão, D. (1999). Detection of siderophore production from several fungi and bacteria by a modification of chrome azurol S (CAS) agar plate assay. Journal of Microbiological Methods, 37(1), 1–6. https://doi.org/10.1016/S0167-7012(99)00028-7
Mmayi, M. P., & Musyimi, D. M. (2025). Effects of Aluminium Application and Rhizobium Inoculation on Aluminium Accumulation, Nodulation and Yields of Soy beans Grown in Kenya. Agriculture Archives, 4(2), 7–19. https://doi.org/10.51470/AGRI.2025.4.2.07
Montes de Oca, P., Mata, R., & Chaves, M. A. (1996). Estudios de salinidad en la provincia de Guanacaste (Costa Rica) y caracterización de algunos suelos con influencia salina. Agronomía Mesoamericana, 7(2), 77. https://doi.org/10.15517/am.v7i2.24766
Osorio, N. W., & Habte, M. (2001). Synergistic Influence of an Arbuscular Mycorrhizal Fungus and a P Solubilizing Fungus on Growth and P Uptake of Leucaena leucocephala in an Oxisol. Arid Land Research and Management, 15(3), 263–274. https://doi.org/10.1080/15324980152119810
Pahalvi, H. N., Rafiya, L., Rashid, S., Nisar, B., & Kamili, A. N. (2021). Chemical fertilizers and their impact on soil health. In Microbiota and Biofertilizers, Vol 2: Ecofriendly Tools for Reclamation of Degraded Soil Environs (pp. 1–20). Springer International Publishing. https://doi.org/10.1007/978-3-030-61010-4_1
Pla Sentís, I. (2020). Overview of salt-affected areas in Latin America: Physical, social and economic perspectives. In Saline and Alkaline Soils in Latin America: Natural Resources, Management and Productive Alternatives (pp. 3–36). Springer International Publishing. https://doi.org/10.1007/978-3-030-52592-7_1
Portillaϯ, J., Ramírez, R., & Lozano, Z. (2025). Fósforo liberado por bacterias nativas de las rocas fosfóricas de Riecito (Estado Falcón) y Navay (Estado Táchira) en Venezuela. Bioagro, 37(1), 111–122. https://doi.org/10.51372/bioagro371.10
Rees, D. C., Akif Tezcan, F., Haynes, C. A., Walton, M. Y., Andrade, S., Einsle, O., & Howard, J. B. (2005). Structural basis of biological nitrogen fixation. Philosophical Transactions of the Royal Society A: Mathematical, Physical and Engineering Sciences, 363(1829), 971–984. https://doi.org/10.1098/rsta.2004.1539
Reyes, I., Bernier, L., Simard, R. R., & Antoun, H. (1999). Effect of nitrogen source on the solubilization of different inorganic phosphates by an isolate of Penicillium rugulosum and two UV-induced mutants. FEMS Microbiology Ecology, 28(3), 281–290. https://doi.org/10.1111/J.1574-6941.1999.TB00583.X
Samago, T. Y., & Dakora, F. D. (2024). Combined use of Rhizobium inoculation and low phosphorus application increased plant growth, root nodulation and grain yield of common bean (Phaseolus vulgaris) in Ethiopia. Frontiers of Agricultural Science and Engineering, 0(0), 0. https://doi.org/10.15302/J-FASE-2024556
Sanga, D. L., Mwamahonje, A. S., Mahinda, A. J., & Kipanga, E. A. (2024). Soil salinization under irrigated farming: A threat to sustainable food security and environment in semi-arid tropics. Journal of Agricultural Science and Practice, 9(3), 32–47. https://doi.org/10.31248/JASP2024.468
Shome, S., Barman, A., & Solaiman, Z. M. (2022). Rhizobium and Phosphate Solubilizing Bacteria Influence the Soil Nutrient Availability, Growth, Yield, and Quality of Soybean. Agriculture, 12(8), 1136. https://doi.org/10.3390/agriculture12081136
Sigma-Aldrich. (2013). P1602 Pikovskaya’s Agar. Product Information. https://www.sigmaaldrich.com/deepweb/assets/sigmaaldrich/product/documents/191/794/p1602dat.pdf
Silva, C. R., Pereira, R. B., & Sabadini, E. (2001). Color changes in indicator solutions: An intriguing and elucidative general chemistry experiment. Journal of Chemical Education, 78(7), 939–940. https://doi.org/10.1021/ED078P939/SUPPL_FILE/JCE2001P0939W.ZIP
Singh, M., Jha, S., Pathak, D., & Maisnam, G. (2025). Advancing biofertilizers: the evolution from single-strain formulations to synthetic microbial communities (SynCom) for sustainable agriculture. Discover Plants 2025 2:1, 2(1), 226-. https://doi.org/10.1007/s44372-025-00318-w
Singh, P., Kumar, V., & Agrawal, S. (2014). Evaluation of phytase producing bacteria for their plant growth promoting activities. International Journal of Microbiology, 2014. https://doi.org/10.1155/2014/426483
Sulistiyani, T. R., Meliah, S., -, M., Kusmiati, M., Budiyanto, A., & Muslichah, D. A. (2024). Molecular Approach and Preliminary Screening of Culturable Free-Living Rhizobium as Plant Growth Enhancer. Malaysian Journal of Science, 43(2), 21–29. https://doi.org/10.22452/mjs.vol43no2.3
Timofeeva, A. M., Galyamova, M. R., & Sedykh, S. E. (2023). Plant Growth-Promoting Soil Bacteria: Nitrogen Fixation, Phosphate Solubilization, Siderophore Production, and Other Biological Activities. Plants 2023, Vol. 12, Page 4074, 12(24), 4074. https://doi.org/10.3390/PLANTS12244074
Utsumi, N., & Kim, H. (2022). Observed influence of anthropogenic climate change on tropical cyclone heavy rainfall. Nature Climate Change, 12, 436–440. https://doi.org/10.1038/s41558-022-01344-2
Verma, D. K., Pandey, A. K., Mohapatra, B., Srivastava, S., Kumar, V., Talukdar, D., Yulianto, R., Zuan, A. T. K., Jobanputra, A. H., & Asthir, B. (2019). Plant Growth-Promoting Rhizobacteria: An Eco-Friendly Approach for Sustainable Agriculture and Improved Crop Production. In Microbiology for Sustainable Agriculture, Soil Health, and Environmental Protection (pp. 3–80). Apple Academic Press. https://doi.org/10.1201/9781351247061-1
Waring, B. G., De Guzman, M. E., Du, D. V., Dupuy, J. M., Gei, M., Gutknecht, J., Hulshof, C., Jelinski, N., Margenot, A. J., Medvigy, D., Pizano, C., Salgado-Negret, B., Schwartz, N. B., Trierweiler, A. M., Van Bloem, S. J., Vargas G., G., & Powers, J. S. (2021). Soil biogeochemistry across Central and South American tropical dry forests. Ecological Monographs, 91. https://doi.org/10.1002/ecm.1453
Wekesa, C., Asudi, G. O., Okoth, P., Reichelt, M., Muoma, J. O., Furch, A. C. U., & Oelmüller, R. (2022). Rhizobia Contribute to Salinity Tolerance in Common Beans (Phaseolus vulgaris L.). Cells, 11. https://doi.org/10.3390/cells11223628
