|
|
COMUNICACIÓN BREVE
Detección molecular y serológica de Trypanosoma cruzi en un gato doméstico de Costa Rica
María J. Zuniga-Moya1,2![]() , Vanessa Robles–Cruz1
, Vanessa Robles–Cruz1![]() , Mauricio Jiménez-Soto3
, Mauricio Jiménez-Soto3![]() , Marta C. Bonilla-González2
, Marta C. Bonilla-González2![]() & Gaby Dolz1,2
& Gaby Dolz1,2![]()
1. Universidad Nacional de Costa Rica, Maestría en Enfermedades Tropicales, Posgrado Regional Ciencias Veterinarias Tropicales, Heredia, Costa Rica; maria.zuniga.moya@una.ac.cr, vanerc09@gmail.com 2. Universidad Nacional de Costa Rica, Laboratorio de Zoonosis y Entomología, Programa Medicina Poblacional (MEDPOB), Escuela de Medicina Veterinaria, Heredia, Costa Rica; marta.bonilla.gonzalez@una.ac.cr, gaby.dolz.wiedner@una.ac.cr 3. Universidad Nacional de Costa Rica, Hospital de Especies Menores y Silvestres (HEMS), Escuela de Medicina Veterinaria, Heredia, Costa Rica; mauricio.jimenez.soto@una.ac.cr
Recibido 20-XI-2025 ● Corregido 02-III-2026 ● Aceptado 18-III-2026
DOI: https://doi.org/10.22458/urj.v18i1.6217
ABSTRACT. “Molecular and serological detection of Trypanosoma cruzi in a domestic cat from Costa Rica.” Introduction: Trypanosoma cruzi is the protozoan that causes Chagas disease, a zoonotic infection of major relevance in Latin America. Dogs are the main peridomestic reservoirs, and the role of cats has been less explored. Objective: To check for T. cruzi in domestic cats from Costa Rica's Central Valley as a baseline for its possible role in urban and peridomestic infection cycles. Methods: We analyzed serum and DNA from 155 cats collected in mid-2021 using Indirect Hemagglutination (IHA), Indirect Fluorescent (IFA), and PCR assays. Results: One cat (0,6%) tested positive across all three platforms. Genetic sequencing revealed a 100% identity match with a rodent-derived strain from Texas (GenBank: LT220278). Conclusion: Our detection of a confirmed T. cruzi infection in a domestic cat demonstrates that the parasite is present in very low levels in some Costa Rican urban environments.
Keywords: Trypanosoma cruzi, Chagas disease, American tripanosomiasis, domestic cats, zoonosis, PCR.
RESUMEN. Introducción: Trypanosoma cruzi es el protozoo causante de la enfermedad de Chagas, una infección zoonótica de relevancia en América Latina. Los perros son los principales reservorios peridomésticos, el papel de los gatos ha sido menos explorado. Objetivo: investigar la presencia de T. cruzi en gatos domésticos del Valle Central de Costa Rica como base de su posible papel en los ciclos de infección urbanos y peridomésticos. Métodos: analizamos el suero y el ADN de 155 gatos recolectados a mediados de 2021 mediante ensayos de Hemaglutinación Indirecta (HAI), Inmunofluorescencia Indirecta (IFI) y PCR. Resultados: un gato (0,6%) resultó positivo en las tres plataformas. La secuenciación genética reveló una identidad del 100% con una cepa derivada de roedores de Texas (GenBank: LT220278). Conclusión: nuestra detección de una infección confirmada por T. cruzi en un gato doméstico demuestra que el parásito está presente en niveles muy bajos en algunos entornos urbanos de Costa Rica.
Palabras clave: Trypanosoma cruzi, enfermedad de Chagas, tripanosomiasis americana, gatos domésticos, zoonosis, PCR.
La enfermedad de Chagas, causada por Trypanosoma cruzi, afecta a humanos y diversos mamíferos y es endémica en Centro y Sudamérica (Durães-Oliveira et al., 2024). En Costa Rica el principal vector doméstico y peridoméstico reportado es Triatoma dimidiata (Argüello-Sáenz, 2018). Aunque la investigación nacional se ha centrado principalmente en humanos y perros (Bonilla et al., 2018), Zeledón et al. (1975), documentaron infección en gatos domiciliados en zonas rurales, lo que evidencia exposición al parásito en escenarios domésticos. Sin embargo, la detección de infección en una especie no implica necesariamente que actúe como reservorio, debido a que esto requiere demostrar parasitemias en concentraciones relevantes y sostenidas, y patrones de contacto que permitan la infección eficiente de triatominos. En gatos, la infección por T. cruzi suele cursar de forma asintomática o con signos poco evidentes, lo que dificulta su detección; en casos crónicos se han descrito manifestaciones cardíacas como miocarditis, arritmias e insuficiencia cardíaca (Zecca et al., 2020; Freitas et al., 2022). Por ello, en ausencia de evidencia directa de infectividad hacia el vector, los gatos deben considerarse principalmente como hospedadores susceptibles y marcadores de exposición en el ambiente doméstico/peridoméstico y su contribución epidemiológica probablemente varía según el contexto ecológico (Gürtler et al., 2006; Jiménez-Coello et al., 2012). De hecho, en México se han reportado prevalencias felinas de hasta 17%, lo que sugiere exposición frecuente, aunque no define por sí sola su papel como reservorio (Jiménez-Coello et al., 2012). En este marco, el presente estudio busca aportar evidencia local mediante técnicas serológicas y moleculares para detectar T. cruzi en los gatos domésticos del Valle Central de Costa Rica sin asumir a priori su rol como reservorios, sino como parte del panorama de exposición doméstica y peridoméstica.
Analizamos un banco de sueros y ADN de 155 gatos recolectados entre mayo y agosto de 2021 en el Valle Central, originalmente obtenido en el marco de un estudio sobre protoparvovirus (Obando-Corella et al., 2024). Las muestras correspondieron a gatos domésticos con propietario, procedentes de clínicas veterinarias (n=20, 12,9%), campañas de castración (n=120, 77,4%) y hogares (n=15, 9,7%). En todos los casos registramos los siguientes datos: fecha de recolecta, identificación del animal, sexo, edad, raza, antecedentes de vacunación, ambiente de residencia (urbano o rural), convivencia con otros gatos, estado de salud, presencia de enfermedades crónicas, estilo de vida (interior o exterior) y lugar de procedencia, además, los animales incluidos en campañas de castración recibieron evaluación clínica al momento del muestreo. En consecuencia, no incluimos gatos callejeros sin propietario. Por tratarse de un análisis secundario de un biobanco previamente establecido, los resultados deben interpretarse dentro del contexto de una población clínica urbana y no como un muestreo poblacional diseñado específicamente para T. cruzi. Las muestras se almacenaron a –20°C hasta su procesamiento (Obando-Corella et al., 2024). La detección serológica se realizó mediante hemaglutinación indirecta (HAI), utilizando el ensayo de Laboratorios Wiener (Rosario, Argentina) con diluciones 1:8–1:256; las muestras reactivas (≥1:32) se confirmaron por inmunofluorescencia indirecta (IFI) (≥1:64), siguiendo a Bonilla et al. (2018). Para la detección molecular se empleó la reacción en cadena de la polimerasa (PCR) anidada dirigida a un segmento de 667pb del gen 18S rRNA de T. cruzi, utilizando los cebadores descritos por Noyes et al. (1999). Los amplicones se enviaron a Macrogen Inc. (Corea del Sur) para secuenciación. Editamos los cromatogramas en BioEdit v7.2.5 y generamos una secuencia consenso. Posteriormente, comparamos la secuencia consenso mediante BLASTn (NCBI), utilizando el algoritmo nucleótido BLAST contra la base de datos de nucleótidos no redundante (nr/nt) de GenBank con los parámetros predeterminados. Para la identificación taxonómica consideramos los mejores alineamientos (mayor bit score y menor E-value) y establecimos como criterio valores superiores al 99%, tanto para el porcentaje de identidad como para la cobertura de alineamiento. Este enfoque se utilizó para confirmación taxonómica a nivel de especie, debido a la naturaleza conservada del 18S rRNA esta región no permite una asignación robusta de DTU.
Un gato (0,6%) resultó positivo en todas las pruebas diagnósticas. Establecimos un título de 1:32 en IHA y de 1:256 en IFI. La secuencia que obtuvimos (GenBank: PV298048) presentó 100% de identidad (632pb/632pb) con una secuencia reportada a partir de un roedor en Texas, EE. UU. (LT220278). El análisis filogenético ubicó la secuencia dentro del clado correspondiente a T. cruzi, agrupándose con secuencias previamente reportadas en América (Fig. 1). La muestra provenía de un macho castrado sin raza definida, entre 1–5 años, que vivía solo en un hogar urbano de la provincia de Alajuela y tenía acceso al exterior; en el examen clínico resultó positivo a virus de leucemia felina (FeLV) y se clasificó como no saludable con anemia sin leucopenia.
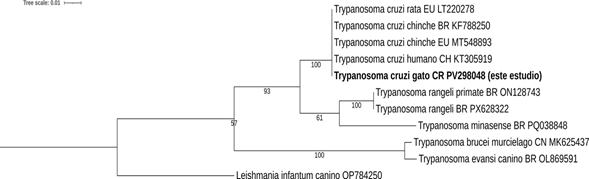
Fig. 1. Árbol filogenético inferido a partir de la secuencia parcial de Trypanosoma cruzi obtenida en este estudio y de secuencias de referencia recuperadas de GenBank. El árbol se construyó mediante el método de Máxima Verosimilitud, utilizando el modelo de sustitución nucleotídica Tamura–Nei. Los valores de bootstrap (1000 réplicas) se muestran en los nodos y solo se presentan aquellos ≥50%. La secuencia generada en este estudio se indica en negrita. Las secuencias del género Leishmania se utilizaron como grupo externo. Los números de acceso de GenBank y el país de origen (abreviado) se indican junto al nombre de cada secuencia. Abreviaturas de países: BR = Brasil, CH = Chile, CN = China, CO = Colombia, CR = Costa Rica, EU = Estados Unidos, MX = México.
El hallazgo de un solo gato positivo coincide con estudios previos en Costa Rica, en donde se ha reportado baja seroprevalencia en caninos (1,17%) (Bonilla et al., 2018). Hasta donde sabemos, este constituye el primer caso confirmado molecularmente de infección por T. cruzi en un gato doméstico en Costa Rica y, probablemente, el primero reportado en Centroamérica. En el estudio de Zeledón et al. (1975) los gatos provenían de zonas rurales con colonización intradomiciliaria activa de Triatoma dimidiata, lo que facilitaba un contacto estrecho entre vectores, roedores y felinos. En contraste, en el Valle Central, la urbanización, el control vectorial y las mejores condiciones habitacionales han reducido la presencia del vector dentro de las viviendas y, por ende, la exposición de los gatos urbanos. Estudios en otros países también muestran esta variación geográfica, como en México, en donde se han encontrado prevalencias considerables de infección felina en contextos urbanos y periurbanos (Jiménez-Coello et al., 2012) y en Venezuela, en donde se han reportado prevalencias superiores al 40% en áreas rurales con ciclos domésticos activos (Díaz-Bello et al., 2022). No obstante, estas prevalencias deben compararse con cautela, dado que los estudios difieren en el tipo de prueba serológica empleada (ELISA, IFI, IHA), antígenos, puntos de corte, así como en el diseño de muestreo (clínico vs comunitario; urbano vs rural), lo que puede influir de manera importante en las estimaciones (Alfonso et al., 2012). Con respecto a la estrategia diagnóstica, utilizamos IHA e IFI porque estas pruebas forman parte del panel serológico disponible para el biobanco analizado y han sido ampliamente empleadas en el diagnóstico serológico de T. cruzi (p. ej., IHA/IFI/ELISA como pruebas de uso frecuente en algoritmos serológicos). Además, la aplicación combinada de dos pruebas serológicas puede aumentar la especificidad, especialmente en regiones con circulación de otros tripanosomátidos como Leishmania (Freitas et al., 2022). Reconocemos; sin embargo, que no realizamos una validación formal específica de desempeño de IHA en sueros felinos dentro de este estudio; por ello, interpretamos los resultados serológicos de manera conservadora y los complementamos con confirmación molecular. En este sentido, la integración de serología y PCR, como en este estudio, permite detectar infecciones en diferentes fases (Tenney et al., 2014; Curtis-Robles et al., 2017) y reduce el riesgo de conclusiones basadas en una sola prueba. Cabe señalar que en los estudios de campo en perros y gatos se han empleado combinaciones de ELISA e IHA junto con herramientas parasitológicas/moleculares, lo que apoya el uso de aproximaciones serológicas combinadas en esta especie, aunque la comparabilidad entre ensayos depende del antígeno y del punto de corte utilizado (Enriquez et al., 2013). La secuencia obtenida mostró identidad con una secuencia previamente reportada de un roedor de Texas; empero, debido a que el marcador 18SrRNA utilizado es principalmente confirmatorio a nivel de especie y no permite asignación robusta de DTU y, considerando que se trata de un único caso, no es posible realizar inferencias sobre linajes circulantes ni sobre rutas específicas de transmisión. Si bien, este hallazgo confirma exposición e infección por T. cruzi en un gato doméstico del Valle Central, no permite inferir su papel epidemiológico en la transmisión local. Es importante señalar que la condición de reservorio implica no solo la infección del hospedador, sino también su capacidad de mantener el parásito y contribuir a la infección de vectores susceptibles. Por lo tanto, este estudio únicamente confirma la susceptibilidad de los gatos a la infección en un contexto urbano y resalta la necesidad de estudios con mayor tamaño muestral y diseño epidemiológico específico, idealmente estratificados por entorno (urbano, periurbano y rural) y estilo de vida (interior/exterior), así como comparaciones con otras especies domésticas potencialmente expuestas. Nuestro resultado resalta la necesidad de estudios con mayor tamaño muestral para evaluar con mayor precisión la frecuencia de infección y explorar su posible relevancia epidemiológica. Futuros trabajos deberían incorporar marcadores moleculares adicionales que permitan la tipificación de las unidades de tipificación discreta (DTU) de Trypanosoma cruzi en gatos domésticos, lo cual contribuiría a una comprensión más detallada de la diversidad genética circulante y del contexto epidemiológico de la infección en el ciclo doméstico y peridoméstico en Costa Rica.
AGRADECIMIENTOS
Agradecemos al Proyecto FUNDAUNA “Diagnóstico e Investigación en Medicina Poblacional y Ecosistémica” que financió este estudio.
DECLARACIÓN DE ÉTICA, CONFLICTO DE INTERESES Y FINANCIAMIENTO
Los autores declaran que han cumplido plenamente con todos los requisitos éticos y legales pertinentes, tanto durante la realización del estudio como en la elaboración del manuscrito; que no existen conflictos de interés de ningún tipo; que todas las fuentes de financiamiento están total y claramente indicadas en la sección de agradecimientos y que están plenamente de acuerdo con la versión final editada del artículo. Se ha archivado un documento firmado en los expedientes de la revista.
La declaración de la contribución de cada autor al manuscrito es la siguiente: G.D., V.R.C., M.J.Z.M.: Diseño del estudio. V.R.C., M.J.Z.M. y M.C.B: Desarrollo de las técnicas (PCR y HAI). G.D., V.R.C., M.J.Z.M. y M.C.B.: Análisis e interpretación de resultados. M.J.S.: Provisión de banco de suero. Todos los coautores: preparación y aprobación final del manuscrito.
REFERENCIAS
Afonso, A. M., Ebell, M. H., & Tarleton, R. L. (2012) A systematic review of high quality diagnostic tests for Chagas disease. PLoS Neglected Tropical Diseases,6(11):e1881. https://doi:10.1371/journal.pntd.0001881.
Argüello-Sáenz, M. (2018). Infestación domiciliar y peridomiciliar de Triatoma dimidiata, vector de la enfermedad de Chagas, en una comunidad periurbana en Heredia, Costa Rica [Tesis de Maestría, Universidad Nacional de Costa Rica]. https://repositorio.una.ac.cr/browse/author?scope=0bfcdeb0-be7f-4944-95f3-7787430922e9&value=Arg%C3%BCello%20S%C3%A1enz,%20Milena&authority=91dd7138-e166-4ed9-b94a-ac77a5d53eb5&bbm.return=1
Bonilla, M. C., Herrero-Acosta, M. V., Urbina-Villalobos, A., & Dolz, G. (2018). Detección de anticuerpos contra Trypanosoma cruzi en caninos de Costa Rica. Revista Ciencias Veterinarias, 36, 1. https://doi.org/10.15359/rcv.36-2.1
Curtis-Robles, R., Zecca, I. B., Román-Cruz, V., Carbajal, E. S., Auckland, L. D., Flores, I., Millard, A. V., & Hamer, S. A. (2017). Trypanosoma cruzi (agent of Chagas disease) in sympatric human and dog populations in “colonias” of the lower Rio Grande valley of Texas. American Journal of Tropical Medicine and Hygiene, 96(4), 805-814. https://doi.org/10.4269/ajtmh.16-0789
Díaz-Bello, Z., De Noya, B. A., Muñoz-Calderón, A., & Beitia, Y. (2022). Seroprevalencia de infección por Trypanosoma cruzi en perros y gatos en la bioregión centro norte de Venezuela. Boletín de Malariología y Salud Ambiental, 62(5), 908-918. https://doi.org/10.52808/BMSA.7E6.625.004
Durães-Oliveira, J., Palma-Marques, J., Moreno, C., Rodrigues, A., Monteiro, M., Alexandre-Pires, G., Da Fonseca, I. P., & Santos-Gomes, G. (2024). Chagas Disease: A silent threat for dogs and humans. International Journal of Molecular Sciences, 25(7), 3840. https://doi.org/10.3390/ijms25073840
Enriquez, G. F., Cardinal, M. V., Orozco, M. M., Lanati, L., Schijman, A. G., & Gürtler, R. E. (2013). Detection of Trypanosoma cruzi infection in naturally infected dogs and cats using serological, parasitological and molecular methods. Acta Tropica, 126(3), 211–217. https://doi.org/10.1016/j.actatropica.2013.03.001
Freitas, N. E. M., Habib, F. L., Santos, E. F., Silva, Â. A. O., Fontes, N. D., Leony, L. M., Sampaio, D. D., de Almeida, M. C., Dantas-Torres, F., & Santos, F. L. N. (2022). Technological advances in the serological diagnosis of Chagas disease in dogs and cats: a systematic review. Parasites and Vectors, 15(1), 343. https://doi.org/10.1186/s13071-022-05476-4
Gürtler, R. E., Cecere, M. C., Lauricella, M. A., Cardinal, M. V., Kitron, U., & Cohen, J. E. (2006). Domestic dogs and cats as sources of Trypanosoma cruzi infection in rural northwestern Argentina. Parasitology, 134(1), 69-82. https://doi.org/10.1017/s0031182006001259
Jiménez-Coello, M., Acosta-Viana, K. Y., Guzmán-Marín, E., Gómez-Ríos, A., & Ortega-Pacheco, A. (2012). Epidemiological survey of Trypanosoma cruzi Infection in domestic owned cats from the tropical southeast of Mexico. Zoonoses and Public Health, 59(s2), 102-109. https://doi.org/10.1111/j.1863-2378.2012.01463.x
Noyes, H., Stevens, J., Teixeira, M., Phelan, J., & Holz, P. (1999). A nested PCR for the ssrRNA gene detects Trypanosoma binneyi in the platypus and Trypanosoma sp. in wombats and kangaroos in Australia. First International Journal for Parasitology, 29(2), 331-339. https://doi.org/10.1016/S0020-7519(98)00167-2
Obando-Corella, A., Solórzano Morales, A., Jiménez-Soto, M., Dolz, G. (2024). Identificación de genogrupos de protoparvovirus y sus variantes en leucocitos de gatos domésticos del Valle Central de Costa Rica. Revista Ciencias Veterinarias, 42, 1-17. https://doi.org/10.15359/rcv.42-2.1
Tenney, T. D., Curtis-Robles, R., Snowden, K. F. & Hamer, S. A. (2014). Shelter dogs as sentinels for Trypanosoma cruzi transmission across Texas. Emerging Infectious Diseases 20(8), 1323-1326. https://doi.org/10.3201/eid2008.131843
Zecca, I. B., Hodo, C. L., Slack, S., Auckland, L., Rodgers, S., Killets, K. C., Saunders, A. B., & Hamer, S. A. (2020). Prevalence of Trypanosoma cruzi infection and associated histologic findings in domestic cats (Felis catus). Veterinary Parasitology, 278, 109014. https://doi.org/10.1016/j.vetpar.2019.109014
Zeledón, R., Solano, G., Burstin, L., & Swartzwelder, J. C. (1975). Epidemiological pattern of Chagas’ disease in an endemic area of Costa Rica. American Journal of Tropical Medicine and Hygiene, 24(2), 214–225. https://doi.org/10.4269/ajtmh.1975.24.214
