|
|
Efecto insecticida, repelente y antialimentario de cinco extractos botánicos en larvas de gusano cogollero, Spodoptera frugiperda (Lepidoptera: Noctuidae)
Jairo Mora Prendas1![]() , Heiner Rodríguez
Solano2
, Heiner Rodríguez
Solano2![]()
1. Universidad de Costa Rica, sede regional de Guanacaste, recinto de Santa Cruz, Costa Rica;
jairo.mora@ucr.ac.cr
2. Servicio Nacional de Aguas Subterráneas, Riego y Avenamiento -Senara, Cañas Guanacaste, Costa Rica; hrodriguez@senara.go.cr
Recibido 17-XI-2025 ● Corregido 20-I-2026 ● Aceptado 23-I-2026
DOI: https://doi.org/10.22458/urj.v18i1.6209
ABSTRACT. “Insecticidal, repellent, and antifeedant effect of five botanical extracts on Spodoptera frugiperda (Lepidoptera: Noctuidae)”. Introduction: The reliance on synthetic insecticides has disrupted the ecological balance of agricultural insect fauna, promoting the development and resistance of pests such as S. frugiperda. As an environmentally “friendly” alternative, the use of plant extracts is promoted for pest control. Objective: To evaluate the insecticidal, repellent, and antifeedant effects of five botanical extracts on Spodoptera frugiperda larvae under laboratory conditions. Materials and Methods: We carried out three laboratory trials, each with six treatments: T1 = distilled water; T2 = Marigold (Tagetes erecta); T3 = garlic (Allium sativum) + neem (Azadirachta indica); T4 = noni (Morinda citrifolia L.) + juanilama (Lippia alba); T5 = papaya seeds (Carica papaya); and T6 = Gliricidia sepium) + oregano (Origanum vulgare L.), using a completely randomized design with 15 replications. We recorded larval mortality as well as the repellent and antifeedant effects of the treatments. Results: In the insecticidal effect tests, garlic and neem extract (T3) caused the highest larval mortality, with significant differences compared to the other treatments (p = 0,038). Feeding and toxic effect tests had no significant differences; the highest larval mortality occurred with the noni + Juanilama (T4) and Gliricidia + oregano (T6) treatments. Additionally, we did not find an effect of the treatments on larval repellency (p = 0,6831). Conclusion: The garlic and neem extract (T3) showed the highest insecticidal effect; however, we did not observe consistent differences among treatments in the other trials. Other dosages and conditions should be tested.
Keywords: pest insects, secondary metabolites, natural control, laboratory, plant protection.
RESUMEN. Introducción: la dependencia de insecticidas sintéticos ha alterado el equilibrio ecológico de la fauna entomológica agrícola, favoreciendo el desarrollo y la resistencia de plagas como S. frugiperda. Como alternativa, se promueve el uso de extractos vegetales para el control de plagas. Objetivo: evaluamos los efectos insecticidas, repelentes y antialimentarios de cinco extractos botánicos sobre larvas de Spodoptera frugiperda en condiciones de laboratorio. Materiales y métodos: realizamos tres ensayos de laboratorio, en cada uno evaluamos seis tratamientos: T1 = agua destilada, T2 = flor de muerto (Tagetes erecta), T3 = ajo (Allium sativum) + neem (Azadirachta indica), T4 = noni (Morinda citrifolia) + juanilama (Lippia alba), T5 = semillas de papaya (Carica papaya) y T6 = madero negro (Gliricidia sepium) + orégano (Origanum vulgare), con un diseño completamente al azar de 15 repeticiones. Registramos la mortalidad larval, así como los efectos repelentes y antialimentarios de los tratamientos. Resultados: en las pruebas de efecto insecticida encontramos que el extracto de ajo y neem (T3) provocó la mayor mortalidad larval con diferencias significativas respecto a los demás tratamientos (p=0,038). En las pruebas de efecto alimentario y tóxico no hallamos diferencias significativas, observamos la mayor mortalidad larval con los tratamientos de noni + juanilama (T4) y de madero negro + orégano (T6). Tampoco detectamos un efecto de los tratamientos sobre la repelencia larval (p=0,6831). Conclusión: el extracto de ajo y neem (T3) tuvo el mayor efecto insecticida; sin embargo, no observamos diferencias coherentes entre los tratamientos en los demás ensayos. Recomendamos evaluar otras dosis y condiciones experimentales.
Palabras clave: insectos plaga, metabolitos secundarios, control natural, laboratorio, protección de plantas.
__________________________________________________________________________________________________
Por años los insumos sintéticos han facilitado la producción agrícola particularmente en el control de plagas y la nutrición de los cultivos (Altieri & Nicholls, 2012; Food Science and Technology, 2019). No obstante, su aplicación desmedida ha generado significativos desequilibrios ecológicos en los sistemas productivos, comprometiendo la funcionalidad de los ecosistemas y la resiliencia agrícola (Deshmukh et al., 2023; Sánchez-Menjivar et al., 2024; Kariyanna et al., 2024). Entre las consecuencias más relevantes se incluyen: la reducción de enemigos naturales (Ndakidemi, Mtei & Ndakidemi, 2016; Overton et al., 2021; Zilnik et al., 2023), la aparición de nuevas plagas, así como la resurgencia y resistencia de insectos nocivos, entre otros impactos (Cervantes Morant, 2010; Sun et al., 2023; Syed, 2025).
La pérdida de la diversidad en los campos agrícolas y la intensificación productiva (i. e. monocultivos) son detonantes para el desarrollo de insectos fitófagos (Kolmans & Vásquez, 1999; Altieri & Nicholls, 2012; Rusch et al., 2016; Paredes et al., 2021; Ziesche, Ordon, Schliephake & Will, 2024). Al no poseer competidores naturales y contar con exceso de alimento, estos organismos, alcanzan densidades poblacionales que impactan negativamente la producción agrícola (Mao et al., 2021; Ali et al., 2023).
Entre los insectos que afectan negativamente los campos agrícolas se encuentran Spodoptera frugiperda (Smith) (Lepidoptera: Noctuidae), especie cosmopolita que afecta una gran variedad de cultivos. Sus afectaciones han sido reportadas al menos en 353 hospederos (Montezano et al., 2018) con una preferencia por las gramíneas, incluyendo los cultivos de maíz y arroz (Casmuz et al., 2010; Cruz, 2013; Nurkomar et al., 2023). El consumo de follaje por S. frugiperda reduce significativamente el área foliar de las plantas en crecimiento y afecta la calidad de flores y frutos, resultando en daños importantes (Cruz, 2013; Instituto Interamericano de Cooperación para la Agricultura [IICA], 1998; Makgoba et al., 2021; Anjorin et al., 2022; Chisonga et al., 2023).
El control de S. frugiperda se ha basado en productos de toxicidad variada (Valarezo Cely, 2003) que, en algunos casos, originan el surgimiento de organismos resistentes (Morillo & Notz, 2001; Paredes-Sánchez et al., 2021; Khan & Ali, 2025). Una alternativa a los productos sintéticos o tóxicos son los extractos de plantas con propiedades repelentes o insecticidas, utilizados ampliamente en la agricultura orgánica por su bajo impacto en el ambiente y la salud humana (Morales & Negrete, 2003; Castro-Jiménez, 2003; Ngegba et al., 2022). Investigaciones previas han demostrado el potencial de los extractos vegetales para el combate de la plaga. Estudios como los de Figueroa y colaboradores (2019) reportaron una disminución superior al 80 % en la abundancia de S. frugiperda al aplicar semanalmente extractos de neem (Azadirachta indica), ajo (Allium sativum) y juanilama (Lippia alba) en campos de maíz. De manera similar, Mora Prendas y Blanco Metzler (2018) registraron reducciones del 50% en el grado de daño en las parcelas tratadas con extractos vegetales en donde la aplicación de los extractos de ajo (A. sativum), neem (A. indica) y detergente, y ajo (A. sativum), orégano (Origanum vulgare), juanilama (L. alba) y romero (Salvia rosmarinus) mitigaron significativamente el grado de daño en comparación con el tratamiento de control (sin aplicación). Asimismo, Brito et al. (2011) reportan una mortalidad promedio de 67,9% de larvas del segundo estadio, tratadas con dos extractos cetónicos de semillas de papaya. Adicionalmente, en un estudio posterior, estos mismos autores reportan reducciones del 29,9% en la severidad de daño provocado por la plaga en parcelas asperjadas con el extracto de semillas de papaya al 20% (Brito et al., 2013). De manera similar, los extractos etanólicos de plantas nativas como Azadirachta indica y Citrullus colocynthis mostraron actividad insecticida significativa contra S. frugiperda, alcanzando hasta 64% de mortalidad, mientras que Spinetoram logró un 100% (Saleem et al., 2024).
Resultados como los anteriores evidencian el potencial de los extractos vegetales como herramientas de manejo integrado de S. frugiperda. Sin embargo, persisten vacíos en el conocimiento respecto a su eficacia, mecanismos de acción y dosis óptimas. Por ello es que en el presente estudio evaluamos de manera sistemática los efectos antialimentarios, insecticidas y repelentes de cinco extractos botánicos elaborados artesanalmente a partir de plantas locales, en condiciones de laboratorio.
MATERIALES Y MÉTODOS
Realizamos la investigación en el Laboratorio de Entomología de la Universidad de Costa Rica, ubicado en la Finca Experimental de Santa Cruz (FESC), Santa Cruz, Guanacaste, entre agosto y diciembre de 2022.
Con el fin de iniciar el estudio, establecimos un pie de cría en condiciones semicontroladas. Para ello, colectamos larvas de S. frugiperda biotipo maíz en los campos agrícolas de la Finca Experimental de Santa Cruz (FESC). Posteriormente ubicamos las larvas en recipientes de 30mL que contenían un trozo de hoja de maíz en su interior y una tapa de tergal, con el fin de permitir la ventilación. Cada recipiente fue etiquetado con los datos de colecta (fecha y localidad) y monitoreado durante todo el desarrollo larval. Durante este período, alimentamos a los inmaduros con hojas apicales de plantas jóvenes libres de plaguicidas, las cuales reemplazamos cada tres días. Previamente a la emergencia de los adultos, sexamos las pupas y las organizamos en parejas sexuales (machos y hembras). Cada pareja fue introducida en una jaula de reproducción con el objetivo de obtener una segunda generación, las cuales utilizamos para la realización de los ensayos.
Evaluamos cinco extractos botánicos y un tratamiento testigo (TABLA 1) en condiciones de laboratorio para determinar sus efectos insecticidas, repelentes y antialimentarios sobre larvas de S. frugiperda alimentadas con hojas de maíz. Elaboramos los extractos artesanalmente, combinando las plantas de cada tratamiento desde su formulación inicial, con el fin de garantizar una mezcla homogénea de metabolitos y se aplicaron a una concentración de 20mL·L⁻¹ de H₂O.
Para la formulación de los tratamientos seguimos la metodología descrita por Mora y Blanco (2018). Trituramos todas las estructuras vegetales de interés (TABLA 2) en cantidades iguales por especie (500g de cada una) utilizamos un procesador de alimentos modelo 2.5 QT WARING WFP11SW. Previamente pesamos los materiales con una balanza digital marca KERN, modelo EW 6200-2NM y luego colocamos los triturados en baldes plásticos de cuatro galones (uno por tratamiento (TABLA 1)) . Como medio extractor de metabolitos secundarios añadimos melaza a cada balde en proporción 1:1 con los componentes vegetales. Una vez realizada la mezcla cerramos los baldes con un sello de agua durante 15 días. Transcurrido este período retiramos el sello y filtramos cada mezcla para obtener los extractos botánicos, los cuales envasamos en botellas plásticas oscuras y almacenamos en el refrigerador a una temperatura de 2 a 8°C hasta su utilización.
TABLA 1
Tratamientos utilizados en la evaluación del efecto insecticida, repelente y antialimentario de extractos botánicos en S. frugiperda.
|
Tratamiento |
Descripción |
Dosis |
|
T1 |
Testigo absoluto (agua destilada) |
No aplica |
|
T2 |
500g de flor de muerto |
|
|
T3 |
20mL.L-1H2O |
|
|
T4 |
20mL.L-1H2O |
|
|
T5 |
500g de semillas de papaya |
20mL.L-1H2O |
|
T6 |
500g de madero negro + 500g de orégano |
20mL.L-1H2O |
TABLA 2
Plantas utilizadas para la elaboración de extractos botánicos.
|
Orden |
Especie |
Nombre común |
Estructuras utilizadas |
|
Asterales |
Tagetes erecta L. |
Flor de muerto |
Hojas, flores, raíces |
|
Asparagales |
Allium sativum L. |
Ajo |
Dientes frescos |
|
Brassicales |
Carica papaya L. |
Papaya |
Semillas deshidratadas |
|
Gentianales |
Morinda citrifolia L. |
Noni |
Frutos frescos |
|
Fabales |
Gliricida sepium (Jacq.) Kunth ex Walp. |
Madero negro |
Hojas frescas |
|
Lamiales |
Origanum vulgare L. |
Orégano |
Hojas frescas |
|
Lamiales |
Lippia alba (Mill.) N.E.Br. ex Britton & P.Wilson |
Juanilama |
Hojas frescas |
|
Sapindales |
Azadirachta indica A. Juss. |
Neem |
Frutos frescos |
Evaluación de los Extractos Botánicos
1-Efecto insecticida: medimos inicialmente 20mL de cada extracto botánico, los cuales diluimos individualmente en un litro de agua para obtener soluciones con una concentración al 2% de cada extracto. Posteriormente, con ayuda de una micropipeta volumétrica, aplicamos un mililitro de cada dilución sobre el mesonoto de cada larva, individualizada de acuerdo con su tratamiento y repetición correspondiente. Tras la aplicación de los tratamientos registramos diariamente la sobrevivencia de las larvas, anotando su estado (es decir, viva o muerta) en una tabla de Excel®. Consideramos como muertas a aquellas larvas que no presentaron movimiento y que mostraron un cambio de coloración (tejidos oscuros).
El olfatómetro fue fabricado a partir del prototipo utilizado por Pacheco, Blanco y Mora en su estudio realizado en el año 2012 (Fig. 1).
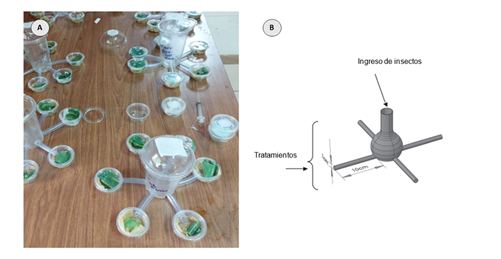 |
Fig.1. Efecto repelente de cinco extractos botánicos sobre larvas de S. frugiperda por medio del olfatómetro. (A) Olfatómetro casero utilizado, (B) Prototipo de Pacheco et al. (2012).
3- Efecto antialimenticio. realizamos ensayos sin libre elección de alimento para evaluar la toxicidad y el efecto antialimenticio de los extractos botánicos en S. frugiperda. Para ello alimentamos directamente a cada larva con hojas de maíz impregnadas con el tratamiento correspondiente (TABLA 1). Registramos diariamente el consumo de alimento, la supervivencia y la mortalidad de las larvas del tercer estadio. Adicionalmente, dejamos 15 individuos sin alimento con el fin de estimar el tiempo de muerte por inanición, el cual fue de nueve días. Al inicio de la prueba, pesamos las larvas no tratadas con una balanza analítica y, de igual forma, registramos el peso de los individuos sobrevivientes al finalizar el experimento.
Análisis Estadístico
Los datos fueron almacenados en una base de datos en Excel®, a partir de la cual se generaron las matrices necesarias para realizar los análisis correspondientes. La normalidad de los datos se evaluó mediante la prueba de Shapiro-Wilk que indicó una distribución no normal. Por lo tanto, se utilizó el test no paramétrico de Kruskal-Wallis para llevar a cabo comparaciones múltiples. Todos los análisis se realizaron utilizando el programa R, versión 3.4.0 (R Core Team, 2017).
RESULTADOS
Encontramos diferencias significativas en las pruebas de efecto insecticida (p = 1,17 × 10⁻⁴) (Fig. 2). El tratamiento T3 (ajo + neem) presentó la mayor mortalidad larval, siendo estadísticamente diferente del resto de los tratamientos (p = 0,038), con un 60% de decesos de S. frugiperda (n = 9). En orden descendente, le siguieron los tratamientos T5 (semillas de papaya) y T6 (madero negro + orégano) con dos muertes registradas en cada uno. Por su parte, tanto T2 (flor de muerto) como el tratamiento testigo (T1) mostraron una sola muerte. En contraste, no se observaron decesos en las larvas expuestas al tratamiento T4 (noni + juanilama). A excepción del T3, ninguno de los restantes tratamientos mostró diferencias significativas entre sí.
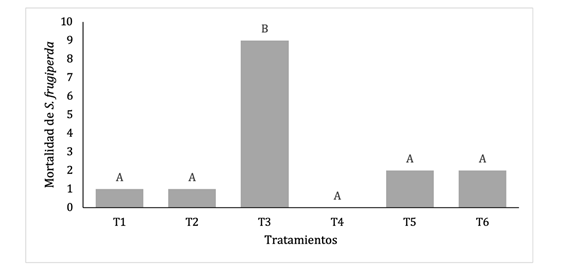
Fig.2. Mortalidad de S. frugiperda (Lepidoptera: Noctuidae) en las pruebas de efecto insecticida con extractos botánicos. Letras distintas indican diferencias significativas (Kruskal Wallis, p<0,05).
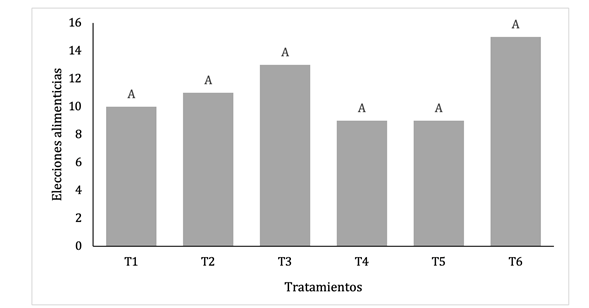 |
Por otra parte, en las pruebas de repelencia realizadas mediante el olfatómetro no encontramos diferencias significativas entre los tratamientos (p = 3,1097). En general, la elección de alimento por parte de S. frugiperda fue similar en todos los tratamientos evaluados (Fig. 3). No obstante, identificamos una leve disminución en la preferencia por los alimentos impregnados con el extracto de noni (T4) y el extracto de semillas de papaya (T5) en comparación con el tratamiento testigo (T1).
Fig.3. Elecciones alimenticias de S. frugiperda (Lepidoptera: Noctuidae) para la evaluación de efecto repelente de extractos botánicos. T1 (testigo), T2 (flor de muerto), T3 (ajo + neem), T4 (noni + juanilama), T5 (semillas de papaya) y T6 (madero negro + orégano). Letras distintas indican diferencias significativas (Kruskal Wallis, p<0,05).
De manera similar al ensayo anterior, en las pruebas de efecto alimenticio no observamos diferencias significativas entre los productos evaluados. Esto se reflejó en el peso final de las larvas (p = 0,416) alimentadas con hojas de maíz impregnadas con los diferentes tratamientos. En todos los casos, los valores fueron similares, excepto en el tratamiento T6 (madero negro + orégano) que presentó la menor ganancia de peso (x̄ = 0,116; TABLA 3).
TABLA 3
Peso promedio de larvas de S. frugiperda al inicio y final de la prueba. T1 (testigo), T2 (flor de muerto), T3 (ajo + neem), T4 (noni) + juanilama), T5 (semillas de papaya) y T6 (madero negro + orégano).
|
Tratamiento |
Peso inicial (gramos) |
Peso final (gramos) |
Significancia |
|
T1 |
0,077 |
A |
|
|
T2 |
0,087 |
0,195 |
A |
|
T3 |
0,096 |
0,192 |
A |
|
T4 |
0,076 |
0,149 |
A |
|
T5 |
0,107 |
0,160 |
A |
|
T6 |
0,097 |
A |
Letras distintas indican diferencias significativas según la prueba de Kruskal Wallis (p< 0,05).
DISCUSIÓN
La efectividad del tratamiento en las pruebas de efecto insecticida a base de ajo y neem (T3) con respecto al testigo puede atribuirse a los compuestos bioactivos presentes en el extracto. El ajo es reconocido como un insecticida sistémico de amplio espectro, capaz de provocar una sobreestimulación del sistema nervioso de los insectos, lo que genera desorientación y reduce su capacidad de alimentación y movimiento (Upadhyay & Singh, 2012; Bordones, De Gracia, Rodríguez, & Chen, 2018). Por su parte, la azadiractina es un metabolito secundario derivado del árbol de neem (Azadirachta indica) que actúa como un regulador del crecimiento en los insectos. Su aplicación interfiere en los procesos de muda y en la síntesis de quitina, provocando deformaciones y alteraciones en el desarrollo de las etapas inmaduras (Sieber & Rembold, 1983; Mordue & Nisbet, 2000; Shu et al., 2021; Fan et al., 2023). Adicionalmente, influye indirectamente en la comunicación sexual y en la fertilidad de los huevos de insectos de los órdenes Lepidoptera y Orthoptera (Cruz, 2004; Ghazawi et al., 2007; Sáenz‑de‑Cabezón Irigaray et al., 2010).
Diversas investigaciones han demostrado la eficacia del extracto de neem (Azadirachta indica) en el control de S. frugiperda. Rahman, Biswas, Barman y Ferdous (2016) reportaron que el extracto etanólico de A. indica presentó una elevada actividad insecticida contra las larvas de esta especie, alcanzando una mortalidad máxima del 64% a una concentración de 400ppm después de 72h de exposición. De manera similar, Hernández-Trejo et al. (2021) evaluaron los compuestos polifenólicos extraídos de las semillas de neem, obteniendo una mortalidad del 60% al emplear un extracto con una dilución 1:12 (m/v) en etanol al 70 %. Igualmente, Kamunhukamwe et al. (2022) evidenciaron que la aplicación de extracto de neem reduce significativamente el daño foliar de la plaga en cultivos de maíz. Por su parte, algunos autores han reportado una eficacia moderada del extracto de ajo contra S. frugiperda, alcanzando una reducción del 54% de la población larval en condiciones de campo (Ceja-Torres, López-Díaz y Gutiérrez-Hernández, 2023). También, Trejo Reyes (2025) indicó que el extracto de ajo aplicado a 100 y 200mL/L fue el tratamiento más efectivo, logrando la mayor reducción del daño causado por S. frugiperda en maíz.
En lo que respecta al efecto antialimenticio y tóxico, ninguno de los tratamientos mostró un impacto significativo en la supervivencia de las larvas de S. frugiperda, lo que sugiere que estas mantuvieron su patrón alimenticio habitual, independientemente del tratamiento aplicado. Estos resultados difieren de los reportados por Tulashie, Adjei, Abraham y Addo (2021), quienes al impregnar hojas de maíz con extractos de neem en concentraciones del 3 y 5% obtuvieron una mortalidad del 100% a las seis horas posteriores a la aplicación del tratamiento. De manera similar, Lin et al. (2021) reportaron una muerte del 51% de larvas, empleando una dosis de 20mg/L. Por otra parte, Sánchez Varela y Rodríguez Luna (2017) confirmaron, en ensayos de laboratorio, las propiedades insecticidas del extracto de noni (M. citrifolia), reportando una mortalidad del 32% en larvas de S. frugiperda cuando fueron alimentadas con 100mL de dieta artificial y 5mL del extracto metanólico del fruto. Este efecto probablemente se deba a la alta concentración de ácido caprílico, un potente antimicótico y ácido caproico con propiedades fungicidas e insecticidas, presentes en todas las partes del fruto (Perales, 2016). De igual manera, otras investigaciones han documentado las propiedades insecticidas del extracto de madero negro (G. sepium). Por ejemplo, Cerda y Jiménez (2012) lograron reducir significativamente las poblaciones de la mosca blanca (Bemisia tabaci) (Hemiptera: Aleyrodidae) en tomate mediante la aplicación de un extracto de hojas de madero negro. Asimismo, Torres y Zamora (2013) reportaron una disminución en las poblaciones de Halticus bracteatus Say (Hemiptera: Miridae) y de B. tabaci al utilizar un extracto combinado de madero negro y chile picante (Capsicum annuum).
Así mismo, algunas investigaciones demuestran el alto potencial que poseen las semillas de papaya para la elaboración de insecticidas naturales. En el año 2013 se evaluaron diferentes concentraciones de extractos metanólicos y hexánicos (cuyo único ingrediente consistió en las semillas de papaya), obteniendo el 100% de las muertes de larvas de Culex tarsalis (Diptera: Culicidae) a las 72 horas posteriores a la aplicación (González Villegas et al., 2013). Dos años después, Gómez (2015) también evaluó diferentes concentraciones de extractos etanoicos de semillas de papaya sobre larvas de Aedes aegypti (Diptera: Culicidae) y encontraron un mayor porcentaje de mortalidad a medida que se aumentaba la concentración del extracto. En otra investigación se obtuvo una mortalidad del 90% de larvas de S. frugiperda que fueron alimentadas con una dieta artificial suplementada con semilla seca triturada de distintas variedades de papaya (Franco Archundia, Jiménez Pérez, Luna León & Figueroa Brito, 2006).
Por otro parte, al analizar el peso final de las larvas, tampoco identificamos diferencias significativas entre tratamientos, estos resultados contrastan con los reportados por Acharya et al. (2023), quienes encontraron una reducción del peso corporal y de la tasa de supervivencia en función de la concentración aplicada de Azadiractina. De manera similar, Salinas‑Sánchez et al. (2012) encontraron que los extractos de Tagetes erecta presentaron actividad bioinsecticida sobre larvas de S. frugiperda, reduciendo su peso y elevando la mortalidad tanto larval como pupal. Igualmente, Pérez-Gutiérrez et al. (2011) demostraron que el extracto de semillas de C. papaya posee efecto insecticida contra la especie, debido a que sus ácidos grasos principales (oleico, palmítico y esteárico) redujeron la viabilidad larvaria, retrasaron el desarrollo del insecto y disminuyeron el peso de las pupas.
Las pruebas de repelencia realizadas mediante el uso del olfatómetro no evidenciaron diferencias significativas entre los tratamientos evaluados. Esto sugiere que ninguno de ellos ejerce un efecto repelente sobre la plaga. No obstante, observamos una tendencia de menor preferencia por los alimentos impregnados con extracto de noni (T4) y con el extracto a base de semillas de papaya (T5), en comparación con el tratamiento testigo (T1), lo que podría sugerir una tendencia biológica relevante, aunque no confirmada estadísticamente.
La limitada eficacia de los extractos observada en esta investigación puede explicarse por la naturaleza intrínsecamente variable de los compuestos bioactivos que los conforman, cuya concentración fluctúa según la sección de la planta empleada y la época de colecta (Zlatić et al., 2019; Tlhapi et al., 2024; AlZunaydi, Alharbi & Alfarhan, 2025). A ello se suma que muchos de estos metabolitos presentan alta volatilidad o se degradan con rapidez, lo que reduce su persistencia y actividad bajo condiciones ambientales no controladas (Clerck et al., 2021; Gupta et al., 2023).
Finalmente, es posible que las dosis aplicadas hayan sido inferiores al umbral biológicamente efectivo, lo cual limitaría su impacto. En conjunto, estos elementos sugieren que los extractos naturales evaluados requieren ajustes en su formulación, concentración y modo de aplicación para consolidarse como alternativas viables dentro de un programa de manejo integrado de la plaga.
AGRADECIMIENTOS
Los autores agradecen a la Universidad de Costa Rica y a la Vicerrectoría de Investigación por financiar el proyecto principal que dio lugar a esta investigación (C0-106 Cuantificación del parasitismo natural de Braconidae e Ichneumonidae (Hymenoptera) en larvas de gusano cogollero del maíz (Spodoptera frugiperda Smith), en Santa Cruz, Guanacaste). Además, expresan su gratitud a Samanta Orellana por su colaboración en la traducción del resumen al inglés.
ÉTICA, CONFLICTO DE INTERESES Y DECLARACIÓN DE FINANCIAMIENTO
Los autores declaramos haber cumplido cabalmente con todos los requisitos éticos y legales pertinentes, tanto durante el estudio como en la producción del manuscrito; que no existen conflictos de intereses de ningún tipo; que todas las fuentes financieras estén completa y claramente indicadas en la sección de agradecimientos y que están totalmente de acuerdo con la versión final editada del artículo. Un documento firmado ha sido archivado en los archivos de la revista.
Contribución de cada autor al manuscrito: J.M.P. y H.R.S. participaron en el diseño del estudio, así como en la recopilación y el análisis de los datos. La recogida de datos fue realizada por ambos autores. Todos los coautores contribuyeron a la preparación y aprobaron la versión final del manuscrito.
REFERENCIAS
Acharya, R., Sharma, S. R., Barman, A. K., Kim, S.-M., & Lee, K.-Y. (2023). Control efficacy of azadirachtin on the fall armyworm, Spodoptera frugiperda (J. E. Smith) by soil drenching. Archives of Insect Biochemistry and Physiology, 112(7), e22020. https://doi.org/10.1002/arch.22020
Ali, M. P., Clemente-Orta, G., Kabir, M. M. M., Haque, S. S., Biswas, M., & Landis, D. A. (2023). Landscape structure influences natural pest suppression in a rice agroecosystem. Scientific Reports, 13, Article 15726. https://doi.org/10.1038/s41598-023-41786-y
Altieri, M. A., & Nicholls, C. I. (2012). Agroecología: Única esperanza para la soberanía alimentaria y la resiliencia socioecológica. Agroecología, 7(2), 65–83. https://revistas.um.es/agroecologia/article/view/182861
AlZunaydi, D. A., Alharbi, A. B., & Alfarhan, A. H. (2025). Impact of season on chemical composition of some medicinal plants in Saudi Arabia. Life, 15(3), 336. https://doi.org/10.3390/life15030336
Anjorin, F. B., Odeyemi, O. O., Akinbode, O. A., & Kareem, K. T. (2022). Fall armyworm (Spodoptera frugiperda) (J. E. Smith) (Lepidoptera: Noctuidae) infestation: Maize yield depression and physiological basis of tolerance. Journal of Plant Protection Research, 62(1), 12–21. https://doi.org/10.24425/jppr.2022.140294
Bordones, A., De Gracia, N., Rodríguez, R., & Chen, A. (2018). Comparación de la efectividad en la protección de cultivos de tomates con insecticidas orgánicos a base de: ajo (Allium sativum) y nim (Azadirachta indica). Revista de Iniciación Científica, 4, 39–42. https://doi.org/10.33412/rev-ric.v4.0.1817
Brito, R. F., Ayala, P. V., Olguín, J. F. L., de la Peña, A. H., Aguilar, J. R. P., & López, M. A. R. (2013). Nitrogen fertilization sources and insecticidal activity of aqueous seeds extract of Carica papaya against Spodoptera frugiperda in maize. Ciencia e Investigación Agraria: Revista Latinoamericana de Ciencias de la Agricultura, 40(3), 578–580. https://doi.org/10.4067/S0718-16202013000300009
Brito, R. F., de la Peña, A. H., Moreno, I. P., Mancebón, V. S. M., & López-Olguín, J. F. (2011). Insecticidal activity of seed extracts of Carica papaya (L.) against the fall armyworm Spodoptera frugiperda (J. E. Smith) (Lepidoptera: Noctuidae). Interciencia, 36(10), 752–756. https://www.redalyc.org/articulo.oa?id=33921449008
Casmuz, A., Juárez, M. L., Socías, M. G., Murúa, M. G., Prieto, S., Medina, S., Willink, E., & Gastaminza, G. (2010). Revisión de los hospederos del gusano cogollero del maíz, Spodoptera frugiperda (Lepidoptera: Noctuidae). Revista de la Sociedad Entomológica Argentina, 69(3‑4), 209–231. https://www.redalyc.org/articulo.oa?id=322028487010
Castro-Jiménez, J. (2003). Determinación, persistencia y distribución de insecticidas de uso agrícola en el medio ambiente (Tesis doctoral, Universidad Autónoma de Madrid). Repositorio de la Universidad Autónoma de Madrid. http://hdl.handle.net/10486/664356
Ceja-Torres, L. F., López-Díaz, S., & Gutiérrez-Hernández, G. F. (2023). Organic extracts for fall armyworm (Spodoptera frugiperda) control in native corn (Zea mays L.). Agro Productividad. https://doi.org/10.32854/agrop.v16i11.2731
Cerda, K. J., & Jiménez-Martínez, E. (2012). Alternativas de manejo contra el complejo mosca blanca (Bemisia tabaci Gennadius)–geminivirus en el cultivo de tomate (Solanum lycopersicum L. = Lycopersicum esculentum Mill.) en Tisma, Masaya (2009) y Camoapa, Boaco (2010). Revista Científica La Calera, 12(18), 18–28. https://doi.org/10.5377/calera.v12i18.1121
Cervantes Morant, R. (2010). Plaguicidas en Bolivia: sus implicaciones en la salud, agricultura y medio ambiente. REDESMA,4(1),27-38.
Chisonga, C., Chipabika, G., Sohati, P. H., & Harrison, R. D. (2023). Understanding the impact of fall armyworm (Spodoptera frugiperda J. E. Smith) leaf damage on maize yields. PLOS ONE, 18(6), e0279138. https://doi.org/10.1371/journal.pone.0279138
Clerck, C., Genva, M., Jijakli, M. H., & Fauconnier, M.-L. (2021). Use of essential oils and volatile compounds as biological control agents. Foods, 10(5), 1062. https://doi.org/10.3390/foods10051062
Cruz, M. (2004). El árbol de nim, establecimiento y aprovechamiento en Huasteca Potosina. Instituto Nacional de Investigaciones Forestales, Agrícolas y Pecuarias. San Luis Potosí, México. p. 8.
Cruz, O. (2013). El cultivo del maíz: manual para el cultivo del maíz en Honduras (3.ª ed.). Dirección de Ciencia y Tecnología Agropecuaria (DICTA), Secretaría de Agricultura y Ganadería (SAG). Tegucigalpa, Honduras. https://dicta.gob.hn/files/2013%2C-Manual-cultivo-de-maiz--G.pdf
Deshmukh, M. S., Ghagare, T. N., Nanaware, D. R., Vadrale, K. S., & Sutar, S. S. (2023). Insumos agrícolas sintéticos y su impacto en los cereales y la salud humana. Journal of Biotechnology and Bioprocessing, 4(2). https://doi.org/10.31579/2766-2314/100
Fan, S.-T., Wu, M.-Z., Liu, C., Li, H.-H., Huang, S.-H., Zheng, Z.-J., Ye, X.-Y., Tan, J.-F., & Zhu, G.-H. (2023). Azadirachtin inhibits nuclear receptor HR3 in the prothoracic gland to block larval ecdysis in the fall armyworm, Spodoptera frugiperda. Journal of Agricultural and Food Chemistry, 71(42), 15497–15505. https://doi.org/10.1021/acs.jafc.3c05508
Figueroa-Gualteros, A., Castro-Triveño, A., & Castro-Zalazar, H. (2019). Efecto bioplaguicida de extractos vegetales para el control de Spodoptera frugiperda en el cultivo de maíz (Zea mays). Acta Biológica Colombiana, 24(1), 64–65. https://doi.org/10.15446/abc.v24n1.69333
Food Science and Technology. (2019). Pesticides in agriculture. Food Science and Technology, 33(1), 52–55. https://doi.org/10.1002/fsat.3301_14.x
Franco‑Archundia, S. L., Jiménez‑Pérez, A., Luna‑León, C., & Figueroa‑Brito, R. (2006). Efecto tóxico de semillas de cuatro variedades de Carica papaya (Caricaceae) en Spodoptera frugiperda (Lepidoptera: Noctuidae). Folia Entomológica Mexicana, 45(2), 171–177. https://www.redalyc.org/pdf/424/42445208.pdf
Ghazawi, N. A., El-Shhranoubi, E. D., El-Shazly, M. M., & Abdel Rahman, K. M. (2007, June 1). Effects of azadirachtin on mortality rate and reproductive system of the grasshopper Heteracris littoralis Ramb. (Orthoptera: Acrididae). Journal of Orthoptera Research, 16(1), 57–65. https://doi.org/10.1665/1082-6467(2007)16[57:EOAOMR]2.0.CO;2
Gómez, N. (2015). Evaluación larvicida del extracto etanólico de la semilla de Carica papaya sobre larvas del IV estadio de Aedes aegypti (Diptera: Culicidae) en condiciones de laboratorio (Tesis de grado, Universidad Distrital Francisco José de Caldas). Universidad Distrital Francisco José de Caldas. https://repository.udistrital.edu.co/items/a0e473b6-6475-4e1e-bdb9-5b3e77daa450
González Villegas, R., Flores Dávila, M., Guerrero Rodríguez, E., Mendoza Villarreal, R., Cárdenas Elizondo, A., Aguirre Uribe, L. A., & Cerna Chávez, E. (2013). Efecto insecticida de extractos vegetales sobre larvas de Culex tarsalis (Diptera: Culicidae) en laboratorio. Revista Mexicana de Ciencias Agrícolas, 4(2), 273–284. https://doi.org/10.29312/remexca.v4i2.1237
Gupta, I., Singh, R., Muthusamy, S., Sharma, M., Grewal, K., Singh, H. P., & Batish, D. R. (2023). Plant essential oils as biopesticides: Applications, mechanisms, innovations, and constraints. Plants, 12(16), 2916. https://doi.org/10.3390/plants12162916
Hernandez-Trejo, A., Rodríguez-Herrera, R., Sáenz-Galindo, A., López-Badillo, C. M., Flores-Gallegos, A. C., & Ascacio-Valdez, J. A. (2021). Insecticidal capacity of polyphenolic seed compounds from neem (Azadirachta indica) on Spodoptera frugiperda (J. E. Smith) larvae. International Journal of Environmental Health Research, 31(9), 1023–1030. https://doi.org/10.1080/03601234.2021.2004853
Instituto Interamericano de Cooperación para la Agricultura (IICA). 1998. Alternativas tecnológicas de producción. Maíz, frijol, arroz, tomate, chile dulce, papa, pepino. IICA, San Salvador, El Salvador. p. 45.
Kamunhukamwe, T., Nzuma, J. K., Maodzeka, A., Gandawa, C. G., Matongera, N., Madzingaidzo, L., & Muturiki, L. (2022). Efficacy of neem bio‑pesticide and synthetic insecticides against control of fall armyworm (Spodoptera frugiperda) in maize. Journal of Entomology and Zoology Studies, 10(4), 1‑6. https://doi.org/10.22271/j.ento.2022.v10.i4b.9018
Kariyanna, B., Senthil-Nathan, S., Vasantha-Srinivasan, P. et al. (2024). Comprehensive insights into pesticide residue dynamics: Unraveling impact and management. Chemical and Biological Technologies in Agriculture, 11, 182. https://doi.org/10.1186/s40538-024-00708-4
Khan, H. A. A., & Ali, A. (2025). First report of field-evolved resistance to insecticides in Spodoptera frugiperda (Lepidoptera: Noctuidae) from Punjab, Pakistan. PLOS ONE, 20(6), e0324857. https://doi.org/10.1371/journal.pone.0324857
Kolmans, E., & Vásquez, D. (1999). Manual de agricultura ecológica: Una introducción a los principios básicos y sus aplicaciones. Grupo de Agricultura Orgánica, Asociación Cubana de Técnicos Agrícolas y Forestales. Ciudad de la Habana, Cuba. pp. 38-40.
Lin, S., Li, S., Liu, Z., Zhang, L., Wu, H., Cheng, D., & Zhang, Z. (2021). Using Azadirachtin to transform Spodoptera frugiperda from pest to natural enemy. Toxins, 13(8), 541. https://doi.org/10.3390/toxins13080541
Makgoba, M. C., Tshikhudo, P. P., Nnzeru, L. R., & Makhado, R. A. (2021). Impact of fall armyworm (Spodoptera frugiperda) (J. E. Smith) on small-scale maize farmers and its control strategies in the Limpopo province, South Africa. Jamba: Journal of Disaster Risk Studies, 13(1), 1016. https://doi.org/10.4102/jamba.v13i1.1016
Mao, Z., Centanni, J., Pommereau, F., Stokes, A., & Gaucherel, C. (2021). Maintaining biodiversity promotes the multifunctionality of social-ecological systems: Holistic modelling of a mountain system. Ecosystem Services, 47, 101220. https://doi.org/10.1016/j.ecoser.2020.101220
Montezano, D. G., Specht, A., Sosa-Gómez, D. R., Roque-Specht, V. F., Sousa-Silva, J. C., Paula-Moraes, S. V., Peterson, J. A., & Hunt, T. (2018). Host plants of Spodoptera frugiperda (Lepidoptera: Noctuidae) in the Americas. African Entomology, 26(2), 286-300. https://doi.org/10.4001/003.026.0286
Mora Prendas, J., & Blanco Metzler, H. (2018). Evaluation of botanical insecticides in controlling the population of fall armyworms (Spodoptera frugiperda Smith) present on corn crops (Zea mays) located in Santa Cruz, Guanacaste. IOP Conference Series: Earth and Environmental Science.
Morales, M., & Negrete, F. (2003). El gusano cogollero del maíz (Spodoptera frugiperda). Corporación Colombiana de Investigación Agropecuaria.
Mordue (Luntz), A. J., & Nisbet, A. J. (2000). Azadirachtin from the neem tree Azadirachta indica: its action against insects. Anais da Sociedade Entomológica do Brasil, 29(4), 615–632. https://doi.org/10.1590/S0301-80592000000400001
Morillo, F., & Notz, A. (2001). Resistencia de Spodoptera frugiperda (Smith) (Lepidoptera: Noctuidae) a lambdacihalotrina y metomil. Entomotropica, 16(2), 79–87.
Ndakidemi, B., Mtei, K., & Ndakidemi, P. A. (2016). Impacts of synthetic and botanical pesticides on beneficial insects. Agricultural Sciences, 7(6). https://doi.org/10.4236/as.2016.76038
Ngegba, P. M., Cui, G., Khalid, M. Z., & Zhong, G. (2022). Use of botanical pesticides in agriculture as an alternative to synthetic pesticides. Agriculture, 12(5), 600. https://doi.org/10.3390/agriculture12050600
Nurkomar, I., Trisnawati, D. W., Fahmi, F., & Buchori, D. (2023). Survival, development, and fecundity of Spodoptera frugiperda (J. E. Smith) (Lepidoptera: Noctuidae) on various host plant species and their implication for pest management. Insects, 14(7), 629. https://doi.org/10.3390/insects14070629
Overton, K., Hoffmann, A. A., Reynolds, O. L., & Umina, P. A. (2021). Toxicity of insecticides and miticides to natural enemies in Australian grains: A review. Insects, 12(2), 187. https://doi.org/10.3390/insects12020187
Pacheco, A., Blanco-Metzler, H., & Mora, R. (2012). Modificación de olfatómetros de cuatro brazos para experimentación en broca del café, Hypothenemus hampei Ferrari (Coleoptera: Curculionidae). Agronomía Costarricense, 36(1), 69–78.
Paredes, D., Rosenheim, J. A., Chaplin-Kramer, R., Winter, S., & Karp, D. S. (2021). Landscape simplification increases vineyard pest outbreaks and insecticide use. Ecology Letters, 24(1), 73-83. https://doi.org/10.1111/ele.13622
Paredes-Sánchez, F. A., Rivera, G., Bocanegra-García, V., Martínez-Padrón, H. Y., Berrones-Morales, M., Niño-García, N., & Herrera-Mayorga, V. (2021). Advances in control strategies against Spodoptera frugiperda: A review. Molecules, 26(18), 5587. https://doi.org/10.3390/molecules26185587
Perales, G. (2016). Estudio de la factibilidad para la creación de una microempresa dedicada a la elaboración de insecticida orgánico a base de semillas de chirimoya y noni en la ciudad de Manta (Tesis de grado). Universidad Laica “Eloy Alfaro” de Manabí. Recuperado de Repositorio Institucional ULEAM
Pérez-Gutiérrez, S., Zavala-Sánchez, M. A., González-Chávez, M. M., Cárdenas-Ortega, N. C., & Ramos-López, M. A. (2011). Bioactivity of Carica papaya (Caricaceae) against Spodoptera frugiperda (Lepidoptera: Noctuidae). Molecules, 16(9), 7502–7509. https://doi.org/10.3390/molecules16097502
R Core Team. (2017). R: A language and environment for statistical computing. R Foundation for Statistical Computing. https://www.R-project.org/
Rahman, S., Biswas, S. K., Barman, N. C., & Ferdous, T. (2016). Plant extract as selective pesticide for integrated pest management. Biotechnological Research, 2(1), 6–10. https://br.biomedpress.org/index.php/br/article /view/706
Rusch, A., Chaplin-Kramer, R., Gardiner, M. M., Hawro, V., Holland, J., Landis, D. A., Thies, C., Tscharntke, T., Weisser, W. W., Winqvist, C., Woltz, M., & Bommarco, R. (2016). Agricultural landscape simplification reduces natural pest control: A quantitative synthesis. Agriculture, Ecosystems & Environment, 221, 198-204. https://doi.org/10.1016/j.agee.2016.01.039
Sáenz‑de‑Cabezón Irigaray, F. J., Moreno‑Grijalba, F., Marco, V., & Pérez‑Moreno, I. (2010). Acute and reproductive effects of Align®, an insecticide containing azadirachtin, on the grape berry moth, Lobesia botrana. Journal of Insect Science, 10(33), 1–11. https://doi.org/10.1673/031.010.3301
Saleem, U., Asrar, M., Jabeen, F., Hussain, S. M., & Hussain, D. (2024). Determination of insecticidal potential of selected plant extracts against fall armyworm (Spodoptera frugiperda) larvae. Heliyon, 10(20), e39593. https://doi.org/10.1016/j.heliyon.2024.e39593
Salinas‑Sánchez, D. O., Aldana‑Llanos, L., Valdés‑Estrada, M. E., Gutiérrez‑Ochoa, M., Valladares‑Cisneros, G., & Rodríguez‑Flores, E. (2012). Insecticidal activity of Tagetes erecta extracts on Spodoptera frugiperda (Lepidoptera: Noctuidae). Florida Entomologist, 95(2), 428‑432. https://doi.org/10.1653/024.095.0225
Sánchez Varela, A., & Rodríguez Luna, I. C. (2017). Mortalidad de larvas de Spodoptera frugiperda por efecto de extractos de fruto de Morinda citrifolia L. (noni). Revista Boliviana de Química, 34(5), 10–12. https://www.redalyc.org/pdf/4263/426354896001.pdf
Sánchez-Menjivar, M., Villalobos-Sequeira, J., Ramírez-Muñóz, F., & Blanco-Peña, K. (2024). Potential pesticide misuse in agriculture farms from two Costa Rican provinces. https://orcid.org/0009-0007-5068-1915
Shu, B., Yu, H., Li, Y., Zhong, H., Li, X., Cao, L., & Lin, J. (2021). Identification of azadirachtin responsive genes in Spodoptera frugiperda larvae based on RNA-seq. Pesticide Biochemistry and Physiology, 172, 104745. https://doi.org/10.1016/j.pestbp.2020.104745
Sieber, K.-P., & Rembold, H. (1983). The effects of azadirachtin on the endocrine control of moulting in Locusta migratoria. Journal of Insect Physiology, 29(6), 523–527. https://doi.org/10.1016/0022-1910(83)90083-5
Sun, S., Zhang, C., Hu, R., & Liu, J. (2023). Do pesticide retailers’ recommendations aggravate pesticide overuse? Evidence from rural China. Agriculture, 13(7), 1301. https://doi.org/10.3390/agriculture13071301
Syed, A. (2025). Pests and pest resistance development: How overuse of pesticides contributes to the evolution of plant pests. Journal of Plant Biochemistry & Physiology, 12, 301. https://doi.org/10.35248/2329-9029.25.13.349
Tlhapi, D., Ramaite, I., Anokwuru, C., van Ree, T., Madala, N., & Hoppe, H. (2024). Effects of seasonal variation on phytochemicals contributing to the antimalarial and antitrypanosomal activities of Breonadia salicina using a metabolomic approach. Heliyon, 10(2), e24068. https://doi.org/10.1016/j.heliyon.2024.e24068
Torres, C., & Zamora, E. (2013). Evaluación de insecticidas botánicos en el manejo de poblaciones de áfidos (Aphis sp.), chinche negro (Halticus bracteatus) y mosca blanca (Bemisia tabaci) en el cultivo de pepino (Cucumis sativus) durante noviembre 2012-enero 2013 (Tesis de grado, Universidad Nacional Autónoma de Nicaragua-León). pp. 11–13.
Trejo Reyes, J. A. (2025). Extractos vegetales para el control del gusano cogollero (Spodoptera frugiperda) en el cultivo de maíz (Zea mays L.). Tecnológico Nacional de México, Instituto Tecnológico Superior de Abasolo. https://rinacional.tecnm.mx/jspui/handle/TecNM/9377
Tulashie, S. K., Adjei, F., Abraham, J., & Addo, E. (2021). Potential of neem extracts as natural insecticide against fall armyworm (Spodoptera frugiperda (J. E. Smith) (Lepidoptera: Noctuidae). Case Studies in Chemical and Environmental Engineering, 4, 100130. https://doi.org/10.1016/j.cscee.2021.100130
Upadhyay, S. K., & Singh, P. K. (2012). Receptors of garlic (Allium sativum) lectins and their role in insecticidal action. Protein Journal, 31(6), 439–446. https://doi.org/10.1007/s10930-012-9423-8
Valarezo Cely, O. (2003). Utilización del nim (Azadirachta indica) en la generación y transferencia de alternativas para el manejo de Spodoptera frugiperda en maíz. Instituto Nacional Autónomo de Investigaciones Agropecuarias. (FAO). Porto viejo, Ecuador. pp 2-3. https://repositorio.iniap.gob.ec/handle/41000/5183
Ziesche, T. M., Ordon, F., Schliephake, E. y Will, T. (2024). Long-term data in agricultural landscapes indicate that insect decline promotes pests well adapted to environmental changes. Journal of Pest Science, 97(3), 1281-1297. https://doi.org/10.1007/s10340-023-01698-2
Zilnik, G., Bergeron, P. E., Chuang, A., Diepenbrock, L., Hanel, A., Middleton, E., Moretti, E., & Schmidt-Jeffris, R. (2023). Meta-analysis of herbicide non-target effects on pest natural enemies. Insects, 14(10), 787. https://doi.org/10.3390/insects14100787
Zlatić, N., Jakovljević, D., & Stanković, M. (2019). Temporal, plant part, and interpopulation variability of secondary metabolites and antioxidant activity of Inula helenium L. Plants, 8(6), 179. https://doi.org/10.3390/plants8060179
