|
|
Producción y caracterización fisicoquímica y textural de biocarbones: influencia del tipo de horno de pirólisis
Irene
Espinoza-Marín1![]() ,
Cristina Chinchilla-Soto2
,
Cristina Chinchilla-Soto2![]() ,
Mayela Monge-Muñoz3
,
Mayela Monge-Muñoz3![]() ,
Wilson Beita-Sandí 4
,
Wilson Beita-Sandí 4![]() & Juan Chin-Pampillo5
& Juan Chin-Pampillo5![]()
1. Universidad de Costa Rica, Centro de Investigación en Contaminación Ambiental (CICA), San José 2060, Costa Rica; irene.esma18@gmail.com
2. Universidad de Costa Rica, Escuela Agronomía, Centro de Investigación en Contaminación Ambiental (CICA), San José 2060, Costa Rica; cristina.chinchilla@ucr.ac.cr
3. Universidad de Costa Rica, Centro de Investigación en Contaminación Ambiental (CICA), San José 2060, Costa Rica; mayela.monge@ucr.ac.cr
4. Universidad de Costa Rica, Escuela Agronomía, Centro de Investigación en Contaminación Ambiental (CICA), San José 2060, Costa Rica; wilson.beita@ucr.ac.cr
5. Universidad de Costa Rica, Escuela Ingeniería de Biosistemas, Centro de Investigación en Contaminación Ambiental (CICA), San José 2060, Costa Rica; juan.chin@ucr.ac.cr
Recibido 11-XI-2025 ● Corregido 05-II-2026 ● Aceptado 09-II-2026
DOI: https://doi.org/10.22458/urj.v18i1.6173
ABSTRACT. “Production and physicochemical and textural characterization of biochars: Influence of the type of pyrolysis system”. Introduction: Biochar is a carbon-based material with strong potential to enhance soil fertility and contribute to agricultural sustainability. Its physicochemical properties depend on both the biomass used and the production conditions. In Costa Rica, crops such as coffee and oil palm generate large volumes of lignocellulosic residues with limited re-use options, representing an opportunity for conversion into biochar. Objective: To evaluate the effect of the pyrolysis system (field kiln and laboratory oven) on the production of biochar from cypress wood (Cupressus sp.), oil palm fruit bunch stalks (Elaeis guineensis), and bamboo (Guadua angustifolia), and its influence on their physical and chemical properties. Methods: Biochars were produced using an open-field "Kon Tiki" kiln and a laboratory-scale muffle furnace under controlled conditions. We characterized the materials using proximate analysis, ash content, pH, and electrical conductivity. Adsorption capacity was assessed using methylene blue and iodine number tests, while surface area and total porosity were estimated by the BET method. Results: We observed significant differences between biochars depending on biomass and kiln type. Field-produced biochars showed higher pH, electrical conductivity, and ash content, which correlated with greater cation exchange capacity but lower structural homogeneity. In contrast, laboratory biochars exhibited higher fixed carbon content, lower volatile-compound fraction, and superior textural development, reflected in larger surface areas and total porosities. The iodine number consistently exceeded methylene blue adsorption, confirming the predominance of the microporous fraction. Conclusions: Both biomass and kiln type strongly influence biochar properties. The methodological adjustments applied to the adsorption analysis improved measurement precision and analytical efficiency, making it suitable for large-sample studies under conventional laboratory conditions.
Keywords: proximal analysis, adsorption, BET, “Kon Tiki” kiln, Costa Rica
RESUMEN. Introducción: el biocarbón es un material carbonoso con potencial para mejorar la fertilidad de los suelos y contribuir a la sostenibilidad agrícola. Sus propiedades fisicoquímicas dependen tanto de la biomasa empleada como de las condiciones de producción. En Costa Rica, cultivos como café y palma africana generan grandes volúmenes de residuos lignocelulósicos con escaso aprovechamiento, lo que representa una oportunidad para su transformación en biocarbón. Objetivo: evaluar el efecto del tipo de horno en la producción de biocarbón a partir de madera de ciprés (Cupressus sp.), pinzote de palma africana (Elaeis guineensis) y bambú (Guadua angustifolia), sobre las propiedades físicas y químicas. Métodos: elaboramos biocarbones en un horno abierto de campo tipo “Kon Tiki” y en un horno de laboratorio tipo mufla bajo condiciones controladas. Caracterizamos los materiales mediante análisis proximal, determinación de cenizas, pH y conductividad eléctrica. La capacidad de adsorción la evaluamos mediante las pruebas de azul de metileno y número de yodo, el área superficial y la porosidad total la estimamos con el método BET. Resultados: observamos diferencias significativas entre los biocarbones según la biomasa y el tipo de horno. Los biocarbones producidos en campo presentaron valores más altos de pH, conductividad eléctrica y cenizas, propiedades asociadas a una mayor capacidad de intercambio catiónico, pero a una menor homogeneidad estructural. En contraste, los biocarbones de laboratorio mostraron mayor contenido de carbono fijo, menor fracción de compuestos volátiles y mejor desarrollo textural, reflejado en áreas superficiales y porosidades totales superiores. El índice de yodo fue consistentemente mayor que la adsorción de azul de metileno, lo que confirma la predominancia de la fracción microporosa. Conclusiones: tanto la biomasa como el tipo de horno influyen de manera determinante en las propiedades del biocarbón que condicionan su desempeño como enmienda agrícola.
Palabras clave: análisis proximal, adsorción, BET, horno “Kon Tiki”, Costa Rica
El uso del biocarbón como enmienda agrícola se remonta a más de dos mil años con evidencia destacada en la cuenca del Amazonas (Gul et al., 2015). En esta región se encuentran las denominadas Tierras Oscuras Amazónicas, suelos antropogénicos formados por la adición recurrente de materiales carbonizados durante siglos, los cuales exhiben una fertilidad excepcional atribuida al alto contenido de carbono estable y a una estructura fina y altamente porosa, comparable a la del biocarbón moderno (Yaashikaa et al., 2020). Estos antecedentes han impulsado el interés contemporáneo en el biocarbón como herramienta para mejorar la calidad del suelo y promover sistemas agrícolas más sostenibles.
En la actualidad, el biocarbón se define como un material carbonoso obtenido por pirólisis de biomasa bajo condiciones controladas, cuya incorporación al suelo puede mejorar la disponibilidad de nutrientes, optimizar la retención de agua e incrementar la capacidad de intercambio catiónico (CIC), contribuyendo así a la fertilidad agrícola (Singh et al., 2017). Además, su uso puede favorecer el secuestro de carbono y reducir emisiones de gases de efecto invernadero como el óxido nitroso, consolidándose como una estrategia de mitigación y adaptación al cambio climático (Lehmann & Joseph, 2015; Enebe et al., 2025; Murtaza et al. 2025).
En el contexto costarricense, el manejo de residuos lignocelulósicos representa tanto un desafío como una oportunidad para la sostenibilidad agrícola y forestal. Cultivos de importancia económica, como la palma africana (Elaeis guineensis Jacq.), generan grandes volúmenes de subproductos, entre el pinzote de palma africana, cuyo aprovechamiento es aún limitado (Soto-Muñoz, 2025, Chin-Pampillo, 2021; Concilco et al., 2018; Hojah, 2013). Paralelamente, Costa Rica cuenta con plantaciones forestales comerciales, particularmente de ciprés (Cupressus sp.), así como con un creciente uso de bambú (Guadua angustifolia) en sistemas agroforestales, construcción sostenible y restauración ecológica, lo que genera residuos leñosos y lignocelulósicos con potencial para su valorización mediante pirólisis. Estos tres tipos de biomasa representan matrices contrastantes en términos de composición anatómica, contenido de lignina y fracción mineral, lo que las convierte en modelos adecuados para evaluar cómo la naturaleza del tejido vegetal modula las propiedades finales del biocarbón.
Las propiedades fisicoquímicas y estructurales del biocarbón dependen directamente del tipo de biomasa empleada y de las condiciones de pirólisis, tales como la temperatura, el tiempo de residencia, la atmósfera de reacción y el diseño del reactor o del horno utilizado (Gezahegn et al., 2025; Khater et al., 2024; Dayoub et al., 2024). Si bien, la literatura ha documentado extensamente los efectos de la temperatura y de la materia prima sobre la composición química y estabilidad del biocarbón (Gezahegn et al., 2025; Kadum et al., 2025; Luo et al., 2024; Khater et al., 2024), existe un vacío de conocimiento respecto al impacto específico del tipo de sistema de pirólisis, especialmente la comparación entre hornos de campo y de laboratorio sobre parámetros funcionales claves como la porosidad, la capacidad de intercambio catiónico y la homogeneidad estructural. Esta limitación es particularmente relevante en contextos agrícolas tropicales, en donde las tecnologías de producción a pequeña escala son las más accesibles, pero su desempeño frente a los sistemas controlados ha sido poco evaluado sistemáticamente.
En este sentido, el presente trabajo tiene como objetivo evaluar el efecto del sistema de pirólisis (campo y laboratorio) en la producción de biocarbón a partir de madera de ciprés (Cupressus sp.), pinzote de palma africana (Elaeis guineensis) y bambú (Guadua angustifolia), determinando su impacto sobre propiedades físicas y químicas relevantes para su uso como enmienda agrícola y material funcional. Nuestra hipótesis es que las propiedades fisicoquímicas del biocarbón dependen tanto del tipo de biomasa utilizada como de las condiciones de pirólisis, de manera que los biocarbones producidos en laboratorio podrían presentan una estructura más desarrollada, mayor estabilidad y uniformidad que aquellos obtenidos en condiciones de campo.
MATERIALES Y MÉTODOS
Producción de biocarbón: elaboramos biocarbón a partir de biomasa de (1) madera de ciprés (Cupressus sp.) (CI), (2) pinzote de palma africana (Elaeis guineensis) (P) y (3) bambú (Guadua angustifolia) (B). Realizamos la pirólisis en dos tipos de hornos: (1) un horno abierto tipo “Kon Tiki” en campo (C) con cortina de llama y temperaturas aproximadas entre 500 y 600°C, donde obtuvimos 10kg de cada tipo de biocarbón y (2) un horno de laboratorio (L) tipo mufla operado bajo condiciones controladas a 600°C con un tiempo de residencia de 1h (TABLA 1), donde obtuvimos 500g de cada tipo de biocarbón. Todos los biocarbones, después de ser producidos, se morterizaron y pasaron por tamices número 14 y 20 (apertura de 1,4 y 0,8mm, respectivamente).
TABLA 1
Descripción de combinaciones de biomasa y tipo de pirólisis para obtención de biocarbón
|
Experimento |
Horno |
Biomasa |
Tratamiento |
|
1 |
Campo (Kon Tiki) |
Pinzote de palma |
CP |
|
2 |
Laboratorio (Mufla) |
Pinzote de palma |
LP |
|
3 |
Campo (Kon Tiki) |
Ciprés |
CCI |
|
4 |
Laboratorio (Mufla) |
Ciprés |
LCI |
|
5 |
Campo (Kon Tiki) |
Bambú |
CB |
|
6 |
Laboratorio (Mufla) |
Bambú |
LB |
Caracterización del biocarbón: la selección de las propiedades fisicoquímicas analizadas se fundamentó en su relevancia para evaluar la calidad y funcionalidad del biocarbón en aplicaciones agrícolas y ambientales. El pH y la conductividad eléctrica (CE) se determinaron por su relación directa con la fracción mineral y la capacidad del biocarbón para modificar la acidez y disponibilidad de nutrientes en el suelo, valores elevados de pH (>8) suelen asociarse con mayor alcalinidad y potencial correctivo en suelos ácidos, mientras que CE altas indican mayor contenido de sales solubles. La capacidad de intercambio catiónico (CIC) se evaluó como indicador de la densidad de cargas superficiales activas, vinculadas a la retención de nutrientes y a la interacción con coloides del suelo, siendo valores superiores a 20cmol kg⁻¹ típicamente considerados favorables para aplicaciones agronómicas (Guo, 2020).
El análisis proximal (compuestos orgánicos volátiles (COV), cenizas y carbono fijo (CF)) se empleó para estimar el grado de carbonización y la estabilidad del material. Finalmente, las propiedades texturales, evaluadas mediante la adsorción de azul de metileno (AM), número de yodo y el método BET se utilizaron como indicadores de la microporosidad y área superficial específica, factores determinantes para la adsorción de contaminantes y la capacidad de retención de agua (Chang & Lee, 2024).
pH y CE: mezclamos 10g de biocarbón con 100mL de agua desionizada (relación 1:10 p/v). Agitamos la suspensión durante 1h en un agitador de tubos de 360° (ATR Rotamix RKVSD, Alemania), la centrifugamos durante 5min (Sigma-4K15, Alemania) y la filtramos por gravedad. Analizamos el filtrado en un medidor multiparámetro (Thermo Scientific Orion Star A329, EUA) para determinar pH y CE.
Análisis proximal: determinamos el contenido de COV, cenizas y el contenido de CF. Pesamos 1,0g de biocarbón en crisoles de porcelana y determinamos los COV mediante calentamiento en mufla a 950°C durante 10min y las cenizas mediante calentamiento en mufla a 750°C durante 6h. Después de cada calentamiento, colocamos las muestras en un desecador hasta su enfriamiento y las pesamos para calcular COV (ecuación 1) y cenizas (ecuación 2). Calculamos el contenido de CF por diferencia entre COV y cenizas (ecuación 3).
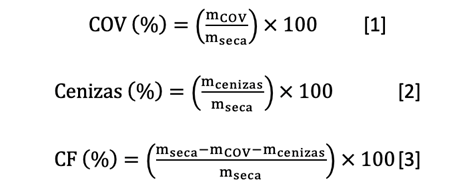 |
Donde, mseca: masa seca de la muestra (g), mCOV: masa correspondiente a la fracción volátil (g), mcenizas: masa de la fracción de cenizas obtenida tras calcinación (g).
Capacidad de Intercambio Catiónico
Aunque el método de capacidad de intercambio catiónico utilizado en este estudio fue originalmente desarrollado para suelos minerales, su adaptación al biocarbón constituye una herramienta útil para evaluar el desarrollo de carga superficial y el potencial de retención de nutrientes. No obstante, los biocarbones difieren de los suelos en su heterogeneidad superficial, contenido de cenizas y composición de grupos funcionales, lo cual puede influir en los valores absolutos de CIC y limitar comparaciones directas con referencias edáficas. Por ello, los resultados de CIC se interpretan principalmente de forma comparativa entre tratamientos más que como indicadores absolutos de desempeño agronómico.
Extracción de amonio: para determinar el contenido de amonio adoptamos el método descrito por Forster (1995) y Verdouw et al. (1978), el cual es un procedimiento para el suelo y no para el biocarbón. Pesamos aproximadamente 5,0g de biocarbón en un Erlenmeyer. Agregamos 50mL de acetato de amonio 1M y agitamos en un Rockin mixer Vibromatic durante 30min. Después de la agitación realizamos una filtración al vacío (Filtro Q2 Fisher Scientific) y dejamos filtrar hasta que no quedara más líquido encima, pero antes de que la muestra se secara y comenzara a agrietarse. Enjuagamos cualquier resto del biocarbón en el Erlenmeyer con una pequeña cantidad de solución de acetato de amonio y agregamos en el filtro, en caso de ser necesario repetimos hasta transferir la mayor cantidad de la muestra. Seguidamente, realizamos cuatro adiciones separadas de aproximadamente 15 a 20mL de etanol al 95% como lavados para eliminar el exceso de acetato de amonio. De la misma manera, se permitió que cada adición se filtrara por completo antes de agregar la siguiente y no se dejó que la muestra se secara. Desechamos la mezcla de acetato de amonio y etanol contenido en el Kitasato. Cambiamos el Kitasato por uno más pequeño para realizar la extracción del amonio adsorbido en el biocarbón mediante lixiviación con cuatro adiciones separadas de 15 a 20mL de cloruro de potasio (KCl) 1M, siguiendo los pasos de filtración indicados anteriormente. Enjuagamos en Kitasato con pequeñas cantidades de KCl, luego transferimos el extracto con KCl del Kitasato a un balón aforado de 100mL que después se aforó. Finalmente, transvasamos a tubos Falcon de 50mL para ser analizado.
Determinación de Amonio-N: elaboramos una solución de amonio de 100ppm (NH4-N). Preparamos una solución estándar de 0,1 a 50ppm, mezclando solución madre y agua desionizada. Preparamos el reactivo A (0,125g de nitroprusiato de sodio, 32,5g de salicilato de sodio, 25g de citrato de sodio y 25g de tartrato de sodio en un balón aforado de 250mL con agua desionizada y se almacenó en una botella oscura en frío) y el reactivo B (disolviendo 15g de hidróxido de sodio en un balón aforado de 250mL con agua desionizada y se le agregaron 5mL de hipoclorito de sodio al 3,5%).
Determinamos la humedad en una balanza y registramos la diferencia de masas de la muestra analizada. Pipeteamos una curva estándar junto con cada conjunto de muestras e incluyendo un blanco de reactivo.
Tomamos una alícuota de 0,04mL del extracto de biocarbón obtenido previamente (o estándar) en un tubo de ensayo y añadimos 1,5mL de reactivo A y 1,5mL de reactivo B. Tapamos el tubo de ensayo e invertimos varias veces para mezclar la solución, colocamos el tubo de ensayo con tapa en oscuridad. Trasvasamos a una cubeta de plástico. Después de transcurrida 1h (± 5min) leímos la absorbancia contra un blanco de reactivo (0ppm) en un espectrofotómetro UV-Vis a 650nm.
Determinación de la CIC: calculamos la CIC a partir de la concentración de amonio determinada en el extracto y expresamos el resultado en cmol (+)/kg de biocarbón seco (ecuación 4).
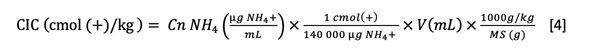 |
Donde Cn NH4 es la concentración de amonio obtenida (ppm), V es el volumen del extracto aforado (100 mL) y MS es la masa seca del biocarbón (g).
Análisis textural del biocarbón: el análisis textural, que comprendió la evaluación de la porosidad y el desarrollo superficial de los biocarbones, se realizó mediante tres enfoques complementarios: adsorción de azul de metileno (AM), determinación índice de yodo (número de yodo, NI) y análisis de área superficial específica por el método Brunauer–Emmett–Teller (BET).
Adsorción de azul de metileno: determinamos la porosidad siguiendo el procedimiento descrito por Nunes y Guerreiro (2011), adaptado al biocarbón. Pesamos 0,300g de muestra de biocarbón en tubos Falcon de 50mL y agregamos 30mL de disoluciones de AM a concentraciones iniciales de 50, 80, 100, 200, 300 y 500mg L-1. Agitamos las muestras durante 24h a temperatura ambiente en un agitador de tubos de 360° (ATR Rotamix RKVSD, Alemania) a velocidad máxima de 80rpm hasta alcanzar el equilibrio y, posteriormente, las centrifugamos durante 40min a 3400–4000rpm (Sigma-4K15, Alemania).
Determinamos la concentración de AM en equilibrio (Ce) mediante espectrofotometría UV-Vis a 645nm, utilizando una curva de calibración (de 0,1 a 5,0mg L-1).
Calculamos la cantidad adsorbida en equilibrio (q_eq, mg g-1) (ecuación 5).
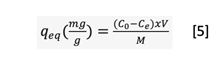 |
Donde C₀ y Cₑ son las concentraciones iniciales y en equilibrio (mg L-1), V el volumen de disolución (L) y M la masa de biocarbón (g).
Con este valor realizamos una isoterma de Langmuir y de Freundlich (ecuaciones 6 y 7), para obtener la adsorción máxima de la muestra analizada.
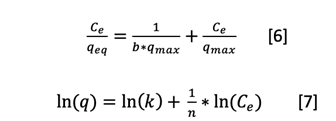 |
Dónde: Ce = concentración de soluto (azul de metileno) en el equilibrio de la fase líquida (mg L−1). qeq = cantidad adsorbida en equilibrio por unidad de masa de adsorbente (biocarbón) (mg g−1). qmax = constante de Langmuir que representa la capacidad máxima de adsorción de la fase sólida (mg g−1). b = constante de Langmuir relacionada con la energía/afinidad de adsorción (proporcional al calor de adsorción) (l mg−1). k = constante de Freundlich de capacidad/afinidad (dependiente del sistema) (mg g−1) (L mg−1)1/n. 1/n = exponente de Freundlich (adimensional).
Índice de yodo: determinamos el índice de yodo según la norma ASTM D4607-94 (ASTM, 2006) y el procedimiento descrito en el GB/T 12496.8-2015 (GB/T, 2015), adaptadas al biocarbón.
Previamente al análisis del biocarbón, estandarizamos las disoluciones de tiosulfato de sodio (Na₂S₂O₃) 0,1N y de yodo 0,1N.
Posteriormente, a 3,0g de biocarbón se adicionaron 10mL de HCl al 5%, lo hervimos durante 30s y lo dejamos enfriar. Añadimos 50mL de disolución de yodo 0,1N y agitamos durante 30min (Rockin mixer, Vibromatic, Francia) a 80rpm. La disolución resultante se filtró por gravedad, tomamos alícuotas de 10,0mL del filtrado y colocamos en Erlenmeyer con 100mL de agua desionizada, titulamos con tiosulfato de sodio 0,1N, utilizando almidón como indicador.
Calculamos el índice de yodo (X/M) (ecuaciones 8 y 9), representando X/M frente a la concentración residual de yodo (C) en escala logarítmica. Utilizamos el valor de X/M correspondiente a C = 0,02N.
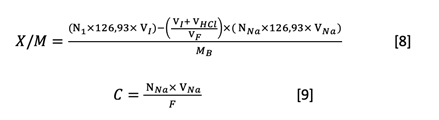 |
Donde NI es la normalidad de la disolución de yodo, VI es el volumen agregado de la disolución de yodo (mL), VHCl es el volumen agregado de HCl al 5% (mL), VF es el volumen de filtrado utilizado en la titulación (mL), NNa es la normalidad de la disolución de tiosulfato de sodio, VNa es el volumen de sodio consumido disolución de tiosulfato (mL), F es el volumen del filtrado que se valora (mL) y MB es la masa de biocarbón (g).
Determinación del área superficial por BET: medimos el área superficial específica mediante adsorción de N₂ siguiendo el método BET. Pesamos 1,0g de biocarbón en un tubo de muestra y determinamos el volumen del sistema utilizando He como gas de referencia. Para la medición de área superficial y porosidad, sustituimos el He por N₂, realizando incrementos de presión de 50 hasta –300mmHg y, posteriormente, de 100–200 hasta alcanzar 0mmHg. Realizamos el cálculo siguiendo los criterios de Walton y Snurr (2007), considerando un área molecular del N₂ de 1,62 × 10⁻¹⁹ m²/molécula. Obtuvimos el volumen total de poro a p/p₀ = 0,98 (p₀ = 658,9mmHg), usando una densidad del N₂ líquido de 0,807g cm-³.
Cálculo de porosidad y área superficial: calculamos los valores de volumen total de porosidad y de área superficial a partir de las ecuaciones 10 y 11, derivadas de los modelos propuestos por Nunes y Guerreiro (2011), utilizando los valores de adsorción máxima de AM y NI:
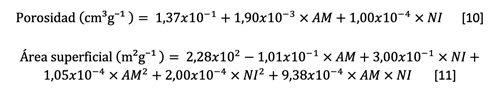 |
Donde AM es la adsorción máxima de azul de metileno (mg g⁻¹), NI es el índice de yodo (mg g⁻¹), Porosidad corresponde al volumen total de poros por unidad de masa (cm³ g⁻¹) y Área superficial corresponde al área superficial específica (m² g⁻¹).
Prueba de pretratamiento del biocarbón: realizamos una prueba para determinar el efecto del pretratamiento con ácido y la reducción del tamaño de partícula sobre la CIC y porosidad, utilizando únicamente biocarbón de bambú producido en campo (CB). Esta matriz fue seleccionada por presentar inicialmente mayor heterogeneidad estructural y menores valores de área superficial, lo que la hacía particularmente sensible a modificaciones físicas y químicas, permitiendo evaluar con mayor claridad el impacto del pretratamiento. Dado que el objetivo fue metodológico (validar el efecto del procedimiento) y no comparativo entre biomasas, se consideró suficiente aplicar el tratamiento a una sola matriz representativa antes de extenderlo al resto de las muestras. El biocarbón de bambú elaborado en campo (CB) tamizado se suspendió en agua desionizada y agregamos ácido clorhídrico (HCl) al 5% gota a gota con agitación hasta alcanzar un pH cercano a 7. Posteriormente, agitamos la suspensión durante 1h y la filtramos al vacío. Secamos completamente el sólido y lo pulverizamos en un molino de bolas (Retsch MM 400, Alemania) durante 7min a 26,1Hz hasta obtener un tamaño fino de partícula que luego tamizamos con una malla N.º 80 (apertura de 0,175mm).
Análisis de datos: evaluamos las diferencias entre tipos de biomasa y hornos utilizados para la producción de biocarbón mediante un enfoque no paramétrico, dado que los datos no cumplieron con el supuesto de normalidad (según prueba de Shapiro-Wilk), además, los tamaños de grupos no fueron uniformes y contamos con un número limitado de réplicas. Estimamos intervalos de confianza al 95% mediante la técnica de Bootstrap, generando distribuciones empíricas del estadístico de interés mediante de remuestreos aleatorios con reemplazo. El análisis se realizó en el software R (versión 1.4.1106), utilizando el paquete boot. La comparación entre tratamientos se efectuó evaluando el grado de superposición entre los intervalos de confianza: cuando el traslape fue mayor al 5% al menos en uno de los puntos de comparación, consideramos que no existían diferencias estadísticamente significativas; por el contrario, cuando el traslape fue inferior al 5% o inexistente, interpretamos que sí existía diferencia significativa. Este criterio se utilizó de manera conservadora como una herramienta exploratoria para identificar tendencias consistentes entre tratamientos más que como una prueba formal de hipótesis, lo cual resulta apropiado para conjuntos de datos pequeños y heterogéneos.
RESULTADOS
Las propiedades fisicoquímicas de los biocarbones mostraron variaciones asociadas tanto al tipo de biomasa como a las condiciones de pirólisis, reflejando el efecto combinado del material de origen y del método de producción sobre su composición y funcionalidad.
Los valores de pH oscilaron entre 7 y 10, situándose en el rango alcalino típico de los biocarbones. Los materiales producidos en campo presentaron valores ligeramente superiores con respecto a los producidos en laboratorio, especialmente el biocarbón de ciprés (CCI, 10,01), seguido del bambú (CB, 10,04). El pinzote de palma mostró el menor pH entre los tratamientos de campo (CP, 7,88) (Fig. 1A).
La CE mostró mayor variabilidad entre tratamientos con valores más altos en los biocarbones de campo, particularmente en bambú (CB, 2137,50 µS cm⁻¹) y pinzote de palma (CP, 1736,26 µS cm⁻¹). En contraste, los biocarbones de laboratorio exhibieron conductividades inferiores (<1000 µS cm⁻¹). Las grandes desviaciones observadas en los materiales de campo evidencian la heterogeneidad de las condiciones de pirólisis (Fig. 1B).
El contenido de cenizas fue mayor en el pinzote de campo (CP, 28,94%), seguido por el ciprés (CCI, 19,80%) y el bambú (CB, 16,49%). Los biocarbones de laboratorio presentaron proporciones menores (<12%) (Fig. 1C).
El contenido de CF fue mayor en los biocarbones producidos en laboratorio de ciprés y pinzote, alcanzando valores cercanos a 81,09 y 80,14%, respectivamente. Por el contrario, el pinzote producido en campo mostró el valor más bajo (46,22%) (Fig. 1D).
Los COV fueron más abundantes en los biocarbones de campo, destacando el pinzote (CP, 24,83%), lo que indica una menor descomposición térmica de los compuestos orgánicos. Los biocarbones de laboratorio presentaron menores contenidos (<15%) con la reducción más notable en el pinzote (LP, 9,85%) (Fig. 1E).
La CIC fue más alta en CP (21,87cmol kg⁻¹), seguida del ciprés de campo (CCI, 12,47cmol kg⁻¹) y del bambú (CB, 11,26cmol kg⁻¹). En los biocarbones de laboratorio, los valores fueron más bajos, aunque más consistentes (2,8 a 4,31cmol kg⁻¹) (Fig. 1F).
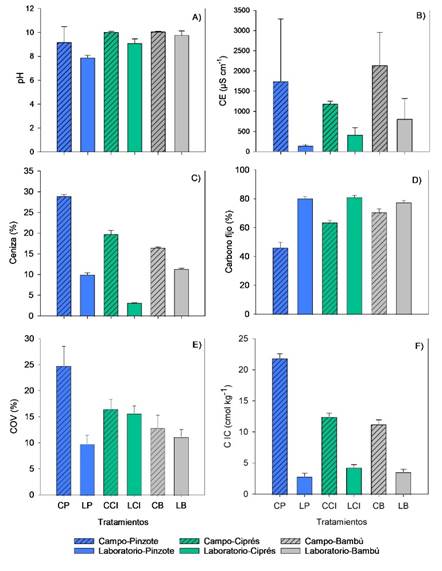
Fig 1. Valores promedio del A) pH, B) conductividad eléctrica (CE, µS cm⁻¹), C) cenizas (%), D) carbono fijo (%), E) compuestos orgánicos volátiles (COV, %), F) capacidad de intercambio catiónico (CIC, cmol kg⁻¹) para biocarbones producidos a partir de distintas biomasas y hornos de pirólisis. Hornos de pirólisis (primera letra): C: horno abierto en campo, L: horno de laboratorio. Biomasas (segunda letra): P: pinzote de palma, CI: ciprés y B: bambú. Las barras verticales representan a la desviación estándar (n = 6).
Con respecto al análisis textural del biocarbón, la capacidad máxima de adsorción de AM (qmax) en los biocarbones de campo presentaron los valores más altos y, en particular, el biocarbón de ciprés (CCI, 16,38mg g⁻¹), contario a esto, los biocarbones de laboratorio presentaron valores bajos y muy similares (5,5-6,6mg g⁻¹, Fig. 2A). El NI fue mayor en los biocarbones de ciprés con valores de 619,68 y 672,76mg I2 g⁻¹, en laboratorio y campo respectivamente (Fig. 2B). Del mismo modo, el área superficial y la porosidad fueron mayor en los biocarbones de ciprés (Fig. 2C, 2D).
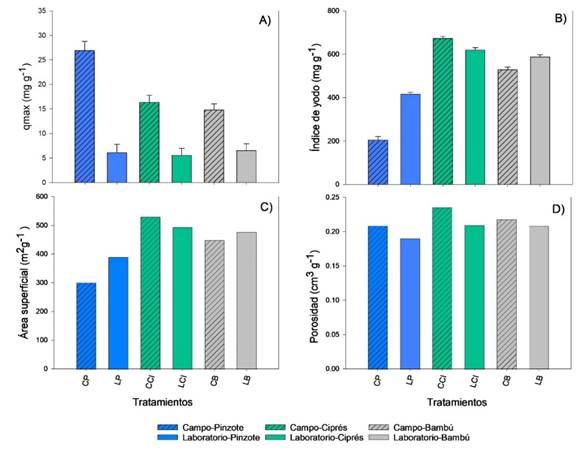
Fig 2. A) capacidad máxima de adsorción de azul de metileno (mg g⁻¹), B) índice de yodo (mg I2 g⁻¹), C) área superficial (m2 g⁻¹) y D) porosidad total (cm3 g⁻¹), determinados para biocarbones de diversas biomasas y hornos de pirólisis por el método de adsorción de azul de metileno. Hornos de pirólisis (primera letra): C: horno abierto en campo y L: horno de laboratorio. Biomasas (segunda letra): P: pinzote de palma, CI: ciprés y B: bambú. Las barras verticales corresponden a la desviación estándar (n= 6).
En el análisis mediante el método BET, las diferencias observadas entre biocarbones fueron más evidentes al comparar el área superficial y la porosidad (Figs. 3A, 3B). Los biocarbones en condiciones de laboratorio de pinzote (LP) y bambú (LB) presentaron valores más altos tanto en área superficial como en porosidad en comparación con los materiales de campo (CP y CB). El biocarbón de ciprés en campo (CCI) destacó con el mayor desarrollo estructural, alcanzando un área superficial de 329,15 ± 1,57m² g⁻¹ y una porosidad de 0,18%.
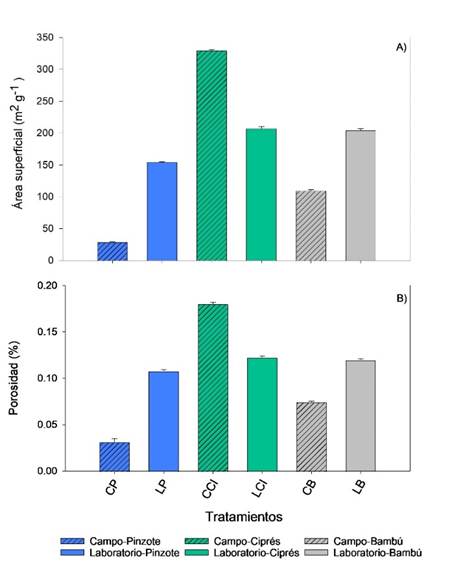
Fig 3. A) área superficial (m² g⁻¹) y B) porosidad (%) determinados para biocarbones de diversas biomasas y hornos de pirólisis mediante el método BET. Hornos de pirólisis (primera letra): C: horno abierto en campo y L: horno de laboratorio. Biomasas (segunda letra): P: pinzote de palma, CI: ciprés y B: bambú. Las barras verticales corresponden a la desviación estándar (n= 6).
Con respecto a la prueba para la aplicación de un pretratamiento, la comparación realizada entre los biocarbones de bambú en campo (CB) con y sin pretratamiento ácido ni tamizado fino permitió evidenciar el efecto de las etapas de acondicionamiento de la biomasa sobre las propiedades estructurales del biocarbón. Aunque ambos materiales fueron obtenidos bajo las mismas condiciones de pirólisis en campo y a partir de la misma materia prima, el biocarbón sin pretratamiento presentó una menor área superficial y porosidad (56,75 ± 2,0m² g⁻¹, 0,047%, respectivamente) en comparación con el biocarbón pretratado (109,67 ± 1,47m² g⁻¹ y 0,075%, respectivamente).
DISCUSIÓN
Los resultados reafirman que tanto el tipo de biomasa como las condiciones de pirólisis influyen significativamente en las propiedades fisicoquímicas y texturales del biocarbón (Dayoub et al., 2024), mostrando diferencias claras entre los materiales producidos en campo y en laboratorio. En términos generales, los biocarbones de campo registraron valores más altos de pH, CE y contenido de cenizas, reflejando una mayor acumulación de fracciones minerales y carbonatos asociada a procesos de pirólisis menos controlados. Este comportamiento coincide con lo reportado por Cornelissen et al. (2017) para hornos Kon-Tiki, en los que los biocarbones de distinta procedencia presentaron CIC elevadas (43–217cmol kg⁻¹) debido al enriquecimiento mineral, aunque con mayor variabilidad estructural. Sin embargo, Masís-Meléndez et al. (2020) observaron que un mayor pH no siempre se traduce en una CIC proporcionalmente más alta, lo que resalta el papel de otros factores como la composición lignocelulósica de la biomasa, el suministro de oxígeno y la geometría del horno.
El efecto de la temperatura de pirólisis fue igualmente determinante. Hadi y Norazlina (2021) demostraron que un incremento de 350 a 750°C en biomasas de palma produce aumentos en pH, CE y nutrientes totales, pero reduce la CIC, mientras que Saputra et al. (2024) reportaron que temperaturas intermedias (≈550°C) y mayores tiempos de residencia (4h) mejoran simultáneamente el pH, la CE y la CIC, al favorecer la transformación gradual de grupos funcionales superficiales. En este estudio, los biocarbones de campo, sujetos a variaciones térmicas, presentaron un patrón similar, en el cual, el aumento del pH y de la CE no siempre implicó una mayor CIC, lo que sugiere que el control de temperatura y tiempo es clave para preservar los sitios activos superficiales responsables del intercambio catiónico.
En relación con el contenido de cenizas, los biocarbones de palma mostraron los valores más elevados, comparado con los de ciprés y bambú. Estas diferencias responden a la naturaleza de los tejidos vegetales: materiales leñosos tienden a generar biocarbones con menores fracciones inorgánicas, mientras que biomasas de rápido crecimiento, como el bambú o los residuos de palma, concentran más minerales (Enders et al., 2012; Leng et al., 2019). Esta fracción mineral es la principal responsable del aumento del pH y de la CE, propiedades deseables para la neutralización de suelos ácidos.
El CF fue mayor en los biocarbones producidos en laboratorio, lo que sugiere una carbonización más eficiente y una matriz más aromática. Esto concuerda con lo descrito por Herviyanti et al. (2022), quienes reportaron que los métodos de pirólisis controlados generan biocarbones más homogéneos y estables. Por el contrario, los biocarbones de campo mostraron menor CF y mayores contenidos de COV, asociados a una combustión incompleta. Este comportamiento ha sido descrito también por Sukiran et al. (2011), quienes reportaron que los biocarbones de palma producidos a bajas temperaturas presentan estabilidad química aceptable, pero escaso desarrollo poroso (áreas BET de 4–6m² g⁻¹).
En cuanto a la CIC, observamos valores más altos en los biocarbones alcalinos producidos en campo, en línea con la correlación positiva entre pH y carga superficial negativa descrita por Chintala et al. (2013) y Singh et al. (2017). No obstante, la elevada variabilidad entre réplicas refuerza la idea de que el control térmico y la uniformidad del flujo de aire influyen directamente en el desarrollo de los grupos funcionales oxigenados responsables de la CIC.
La capacidad máxima de adsorción de AM, como indicador de la disponibilidad de mesoporos y de grupos funcionales superficiales activos, evidenció diferencias notables entre los tratamientos. Los biocarbones de campo mostraron los valores más altos respecto de los biocarbones elaborados en condiciones controladas de laboratorio. Este patrón indica que los materiales generados en hornos abiertos conservan una mayor cantidad de grupos funcionales superficiales activos, favoreciendo la adsorción del AM. En contraste, los biocarbones de laboratorio, aunque más estables, presentan una menor densidad de grupos oxigenados debido al mayor grado de carbonización. Resultados similares han sido descritos por Hadi & Norazlina (2021) y Saputra et al. (2024), quienes reportaron una disminución en la capacidad de adsorción a medida que aumentan la temperatura y la duración del proceso de pirólisis, consecuencia de la pérdida progresiva de grupos polares.
Por otra parte, el índice de yodo mostró valores altos en los biocarbones de ciprés (CCI, LCI) y bambú (CB, LB), con registros superiores a 600mg g⁻¹, seguidos por los de pinzote. Este comportamiento concuerda con lo propuesto por Nunes y Guerreiro (2011), quienes establecen que el yodo, al poseer un tamaño molecular menor, puede acceder con mayor facilidad a los microporos, mientras que el AM se adhiere principalmente a mesoporos. La diferencia entre ambos indicadores sugiere que los biocarbones estudiados poseen una combinación estructural de micro y mesoporos, siendo los de madera los más microporosos. Empero, el análisis del área superficial específica mediante BET mostró una tendencia distinta a la observada con los métodos indirectos. Los biocarbones producidos en laboratorio, especialmente los de ciprés (LCI) y bambú (LB), registraron las áreas superficiales más altas, mientras que los de campo, como el pinzote (CP) y el ciprés (CCI), alcanzaron valores intermedios. Este aumento del área superficial bajo condiciones controladas refleja una carbonización más eficiente y el desarrollo de una red porosa más estable y homogénea. Como lo señalan Alghamdi et al. (2020), el control térmico y la reducción del tamaño de partícula favorecen la exposición de microporos al disminuir la barrera difusiva, lo cual podría explicar los mayores valores BET observados en los tratamientos de laboratorio.
La porosidad total mostró una variación relativamente uniforme entre tratamientos (Fig. 4D), con valores entre 0,18 y 0,22cm³ g⁻¹. Los biocarbones de bambú (CB y LB) y ciprés de campo (CCI) presentaron las porosidades más elevadas, mientras que los de laboratorio de pinzote (LP) mostraron valores ligeramente menores. Este comportamiento sugiere que la estructura porosa global se ve influenciada tanto por la materia prima como por el grado de activación térmica (Tag et al., 2016). Los microporos, generados principalmente durante la pirólisis, aumentan con la temperatura y son responsables de gran parte del área superficial reactiva, mientras que los mesoporos facilitan la difusión hacia estos sitios activos (Escalante et al., 2016). En este sentido, la acción complementaria de microporosidad y mesoporosidad explica la capacidad adsorbente observada, siendo los materiales producidos en laboratorio más estables y con una superficie más desarrollada, mientras que los de campo conservan una mayor reactividad superficial.
La comparación integrada entre los métodos indirectos (NI y adsorción de AM) y el método directo BET permite interpretar con mayor precisión la arquitectura porosa de los biocarbones estudiados. Mientras que el NI reflejó principalmente el desarrollo de microporos, con valores elevados en los biocarbones de ciprés y bambú, la adsorción de AM estuvo más asociada a la disponibilidad de mesoporos y a la presencia de grupos funcionales superficiales activos (Nunes & Guerreiro, 2011). En contraste, el método BET cuantificó el área superficial total accesible, mostrando valores superiores en los biocarbones producidos en laboratorio, especialmente en ciprés y bambú, lo que evidencia una red porosa más estable y homogénea bajo condiciones de pirólisis controladas. Esta divergencia entre métodos indica que un mayor NI o una alta adsorción de AM no necesariamente se traducen en una mayor área superficial BET, sino que reflejan diferentes fracciones de la porosidad funcional del material. Resultados similares han sido reportados por Alghamdi et al. (2020), quienes señalan que los métodos indirectos capturan preferentemente accesibilidad química y microestructura activa, mientras que BET refleja la superficie física total.
La integración de propiedades permitió diferenciar funcionalmente los biocarbones de campo y de laboratorio. Los primeros, por su mayor alcalinidad, cenizas y CIC, son más adecuados como enmiendas agrícolas de efecto inmediato, mientras que los segundos, con mayor carbono fijo y desarrollo poroso, presentan mayor potencial para aplicaciones de largo plazo como adsorción, remediación y secuestro de carbono. Esto resalta la importancia de seleccionar biomasa y condiciones de pirólisis según el uso final del biocarbón.
En conclusión, las propiedades del biocarbón dependen de manera significativa tanto del tipo de biomasa como de las condiciones de pirólisis. Los biocarbones derivados de madera presentaron mayor estabilidad, contenido de carbono fijo y desarrollo estructural, lo que se tradujo en mayores áreas superficiales y capacidad adsorbente, especialmente en los materiales producidos bajo condiciones controladas de laboratorio. Asimismo, la reducción del tamaño de partícula mejoró la exposición de microporos y la eficiencia adsorbente, lo que confirma la importancia de optimizar simultáneamente la biomasa, el sistema de producción y el procesamiento físico en función del uso final del biocarbón.
AGRADECIMIENTOS
Agradecemos el financiamiento recibido de parte del Ministerio de Ciencia y Tecnología de Costa Rica mediante el fondo FI-043B-19 y a la Universidad de Costa Rica, por medio del Proyecto C0-518 BIOECODES: El biocarbón como estrategia de economía circular: valorización de residuos agroindustriales para la descarbonización y la protección de los recursos.
ÉTICA, CONFLICTO DE INTERESES Y DECLARACIÓN DE FINANCIAMIENTO
Declaramos haber cumplido con todos los requisitos éticos y legales pertinentes, tanto durante el estudio como en la producción del manuscrito; que no existen conflictos de intereses de ningún tipo; que todas las fuentes financieras están completa y claramente indicadas en la sección de agradecimientos y que están totalmente de acuerdo con la versión final editada del artículo. Un documento firmado ha sido archivado en los archivos de la revista.
La declaración de la contribución de cada autor al manuscrito es la siguiente: I.E.M y J.S.C.P: diseño del estudio, recopilación y análisis de datos. Todos los coautores: preparación y aprobación final del manuscrito.
REFERENCIAS
Alghamdi, A. G., Alkhasha, A., & Ibrahim, H. M. (2020). Effect of biochar particle size on water retention and availability in a sandy loam soil. Journal of Saudi Chemical Society, 24(12), 1042–1050. https://doi.org/10.1016/j.jscs.2020.11.003
ASTM International. (2006). Standard test method for determination of iodine number of activated carbon (ASTM Standard D4607-94, reapproved 2006). https://doi.org/10.1520/D4607-94
Chang, J., & Lee, J.-Y. (2024). Machine Learning-Based Prediction of the Adsorption Characteristics of Biochar from Waste Wood by Chemical Activation. Materials, 17(21), 5359. https://doi.org/10.3390/ma17215359
Chin-Pampillo, J. S., Alfaro-Vargas, A., Rojas, R., Giacomelli, C. E., Pérez-Villanueva, M., Chinchilla-Soto, C., Alcañiz, J. M., & Domene, X. (2021). Widespread tropical agrowastes as novel feedstocks for biochar production: Characterization and priority environmental uses. Biomass Conversion and Biorefinery, 11(5), 1775–1785. https://doi.org/10.1007/s13399-020-00714-0
Chintala, R., Mollinedo, J., Schumacher, T. E., Papiernik, S. K., Malo, D. D., Clay, D. E., Kumar, S., & Gulbrandson, D. W. (2013). Nitrate sorption and desorption in biochars from fast pyrolysis. Microporous and Mesoporous Materials, 179, 250–257. https://doi.org/10.1016/j.micromeso.2013.05.023
Concilco, E., Moreno, A., García, M., Quiroga, H., & García, O. (2018). Influencia del biocarbón aplicado al suelo sobre atributos de rendimiento y calidad de avena forrajera. Revista Terra Latinoamericana, 36(3), 221–228. https://doi.org/10.28940/terra.v36i3.375
Cornelissen, G., Pandit, N. R., Taylor, P., Pandit, B., Sparrevik, M., & Schmidt, H. P. (2017). Data from: Emissions and char quality of flame-curtain “Kon Tiki” kilns for farmer-scale charcoal/biochar production [Data set]. Dryad. https://doi.org/10.5061/DRYAD.58M67
Dayoub, E. B., Tóth, Z., Soós, G., & Anda, A. (2024). Chemical and Physical Properties of Selected Biochar Types and a Few Application Methods in Agriculture. Agronomy, 14(11), 2540. https://doi.org/10.3390/agronomy14112540
Enders, A., Hanley, K., Whitman, T., Joseph, S., & Lehmann, J. (2012). Characterization of biochars to evaluate recalcitrance and agronomic performance. Bioresource Technology, 114, 644–653. https://doi.org/10.1016/j.biortech.2012.03.022
Enebe, M. C., Ray, R. L., & Griffin, R. W. (2025). The impacts of biochar on carbon sequestration, soil processes, and microbial communities: a review. Biochar, 7(1), 107. https://doi.org/10.1007/s42773-025-00499-3
Escalante-Rebolledo, A., Pérez-López, G., Hidalgo-Moreno, C., López-Collado, J., Campo-Alves, J., Valtierra-Pacheco, E., & Etchevers-Barra, J. D. (2016). Biocarbón (biochar) I: Naturaleza, historia, fabricación y uso en el suelo. Terra Latinoamericana, 34(3), 367–382.
Forster, J. C. (1995). Soil nitrogen. En A. Kassem & N. Paolo (Eds.), Methods in applied soil microbiology and biochemistry (pp. 79–87). Academic Press.
Gezahegn, A., Selassie, Y. G., Agegnehu, G., Addisu, S., Mihretie, F. A., Kohira, Y., & Sato, S. (2025). Pyrolysis temperature changes the physicochemical characteristics of water hyacinth-based biochar as a potential soil amendment. Biomass Conversion and Biorefinery, 15, 3737–3752. https://doi.org/10.1007/s13399-024-05338-2
Gul, S., Whalen, J. K., Thomas, B. W., Sachdeva, V., & Deng, H. (2015). Physico-chemical properties and microbial responses in biochar-amended soils: Mechanisms and future directions. Agriculture, Ecosystems and Environment, 206, 46–59. https://doi.org/10.1016/j.agee.2015.03.015
Guo, M. (2020). The 3R Principles for Applying Biochar to Improve Soil Health. Soil Systems, 4(1), 9. https://doi.org/10.3390/soilsystems4010009
Hadi, A. R. A., & Norazlina, A. S. (2021). The effects of pyrolysis temperature on chemical properties of empty fruit bunch and palm kernel shell biochars. IOP conference series. Earth and environmental science, 757(1), 012029. https://doi.org/10.1088/1755-1315/757/1/012029
Herviyanti, Maulana, A., Lita, A. L., Prasetyo, T. B., & Ryswaldi, R. (2022). Characteristics of biochar methods from bamboo as ameliorant. IOP Conf. Series: Earth and Environmental Science, 959, 1–9. https://doi.org/10.1088/1755-1315/959/1/012036
Hojah, J. (2013). Impacto del uso de biocarbón sobre la calidad de suelos y producción de cacao (Theobroma cacao L.) en sistemas agroforestales, Reserva Indígena Bribri, Talamanca, Costa Rica [Tesis de Maestría, CATIE]. http://www.sidalc.net/repdoc/A10273e/A10273e.pdf
Kadum, A. H., Badin, D. A., Rybakova, S. O., Burakova, I. V., Burakov, A. E., Dyachkova T. P., & Tkachev A. G. (2025). Effect of Carbonization Temperature on the Physicochemical and Sorption Properties of Coals from Plant Biomass for Removing Dyes from Solutions. Inorg. Mater. Appl. Res. 16, 1394–1403 https://doi.org/10.1134/S2075113325701485
Khater, E. S., Bahnasawy, A., Hamouda, R., Sabahy, A., Abbas, W., & Morsy, O. M. (2024). Biochar production under different pyrolysis temperatures with different types of agricultural wastes. Scientific Reports, 14, Artículo 2625. https://doi.org/10.1038/s41598-024-52336-5
Lehmann, J., & Joseph, S. (Eds.). (2015). Biochar for environmental management (2nd ed.). Routledge.
Leng, L., Huang, H., Li, H., Li, J., & Zhou, W. (2019). Biochar stability assessment methods: A review. Science of the Total Environment, 647, 210–222. https://doi.org/10.1016/j.scitotenv.2018.07.402
Luo, Q., Deng, Y., Li, Y., He, Q., Wu, H., & Fang, X. (2024). Effects of pyrolysis temperatures on the structural properties of straw biochar and its adsorption of tris-(1-chloro-2-propyl) phosphate. Scientific Reports, 14, Artículo 25711. https://doi.org/10.1038/s41598-024-77299-5
Masís-Meléndez, F., Segura-Chavarría, D., García-González, C. A., Quesada-Kimsey, J., & Villagra-Mendoza, K. (2020). Variability of physical and chemical properties of TLUD stove derived biochars. Applied Sciences, 10(2), 507. https://doi.org/10.3390/app10020507
Murtaza, G., Abbas, T., Rashid, M., Rizwan, M., Li, S., & Ahmad, S. (2025). Biochar-Soil-Plant Interactions: A Debate on Sustainable Agriculture in the Context of Climate Change. En M. Ahmed (Ed.), Climate Resilient and Sustainable Agriculture (Vol. 2, pp. 79-100). Springer. https://doi.org/10.1007/978-3-032-04141-8_4
Nunes, C. A., & Guerreiro, M. C. (2011). Estimation of surface area and pore volume of activated carbons by methylene blue and iodine numbers. Química Nova, 34(3), 472–476. https://doi.org/10.1590/S0100-40422011000300020
Saputra, I., Prijono, S., Soemarno, & Suntari, R. (2024). Optimization of biochar quality from palm and cacao waste through variation of pyrolysis temperature and duration as a soil amendment material. OnLine Journal of Biological Sciences, 24(4), 765–776. https://doi.org/10.3844/ojbsci.2024.765.776
Singh, B., Camps-Arbestain, M., & Lehmann, J. (2017). Biochar: A guide to analytical methods. CSIRO Publishing. https://books.google.co.uk/books?id=ieRrDgAAQBAJ
Soto-Muñoz, G., Chin-Pampillo, J. S., Villagra-Mendoza, K., & Chinchilla-Soto, C. (2025). Investigación y uso del biocarbón en Costa Rica. Agronomía Costarricense, 49(2), 2907. https://doi.org/10.15517/sh3x5e25
Sukiran, M. A., Kheang, L. S., Bakar, N. A., & May, C. Y. (2011). Production and characterization of biochar from the pyrolysis of empty fruit bunches. American Journal of Applied Sciences, 8(10), 984–988. https://doi.org/10.3844/ajassp.2011.984.988
Tag, A. T., Duman, G., Ucar, S., & Yanik, J. (2016). Effects of feedstock type and pyrolysis temperature on potential applications of biochar. Journal of Analytical and Applied Pyrolysis, 120, 200–206. https://doi.org/10.1016/j.jaap.2016.05.006
Verdouw, H., Van Echteld, C. J. A., & Dekkers, E. M. J. (1978). Ammonia determination based on indophenol formation with sodium salicylate. Water Research, 12(6), 399–402. https://doi.org/10.1016/0043-1354(78)90107-0
Walton, K. S., & Snurr, R. Q. (2007). Applicability of the BET method for determining surface areas of microporous metal-organic frameworks. Journal of the American Chemical Society, 129(27), 8552–8556. https://doi.org/10.1021/ja071174k
Yaashikaa, P. R., Kumar, P. S., Varjani, S., & Saravanan, A. (2020). A critical review on the biochar production techniques, characterization, stability and applications for circular bioeconomy. Biotechnology Reports, 28, e00570. https://doi.org/10.1016/j.btre.2020.e00570
